
科目: 来源: 题型:
下列各项所述的数字不是6的是 ( )。
A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数
B.在金刚石晶体中,最小的环上的碳原子个数
C.在二氧化硅晶体中,最小的环上的原子个数
D.在石墨晶体的片层结构中,最小的环上的碳原子个数
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是 ( )。
A.原子晶体中只存在非极性共价键
B.干冰升华时,分子内共价键会发生断裂
C.由原子构成的晶体可以是原子晶体,也可以是分子晶体
D.只要含有金属阳离子的晶体就一定是离子晶体
查看答案和解析>>
科目: 来源: 题型:
下列性质适合于某种原子晶体的是 ( )。
A.熔点1 070 ℃,易溶于水,水溶液导电
B.熔点10.32 ℃,液态不导电,水溶液导电
C.能溶于CS2,熔点112 ℃,沸点444.6 ℃
D.熔点3 550 ℃,很硬,不溶于水,不导电
查看答案和解析>>
科目: 来源: 题型:
下列各组晶体物质中,化学键类型相同,晶体类型也相同的是 ( )。
①SiO2和SO3 ②晶体硼和HCl ③CO2和SO2 ④晶体硅和金刚石 ⑤晶体氖和晶体氮 ⑥硫黄和碘
A.①②③ B.④⑤⑥
C.③④⑥ D.①③⑤
查看答案和解析>>
科目: 来源: 题型:
下表所列物质晶体的类型全部正确的一组是 ( )。
| 原子晶体 | 离子晶体 | 分子晶体 | |
| A | 氮化硅 | 磷酸 | 单质硫 |
| B | 单晶硅 | 氯化铝 | 白磷 |
| C | 金刚石 | 烧碱 | 冰 |
| D | 铁 | 尿素 | 冰醋酸 |
查看答案和解析>>
科目: 来源: 题型:
《物质结构与性质》从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质。
(1)下列说法正确的是________(填序号)。
A.元素电负性由大到小的顺序为:F>O>N
B.一个苯分子含3个π键和6个σ键
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为:Br>Se>As

(2)根据等电子体原理,羰基硫(OCS)分子的结构式应为________。光气(COCl2)分子内各原子最外层都满足8电子稳定结构,则光气分子的立体构型为________(用文字描述)。
(3)Cu2+基态的电子排布式为____________________________________。
向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4晶体,该物质中配位原子的杂化方式为________。
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素N的基态原子电子排布式:____________________________。
(2)元素B、G形成的单质熔点更高的是________(填化学式),原因是________
________________________________________________________________。
(3)ME2L2常温下为深红色液体,能与 CCl4、CS2 等互溶,据此可判断 ME2L2 是________(填“极性”或“非极性”)分子。根据等电子原理:NO 中氮原子的杂化类型是________;1 mol NO
中氮原子的杂化类型是________;1 mol NO 中含有 π 键的数目为__________。
中含有 π 键的数目为__________。
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的立体构型是________。
查看答案和解析>>
科目: 来源: 题型:
已知 A、D、E、G、L、M 是核电荷数依次增大的6种短周期主族元素,其中 A 的原子序数与周期序数相等,D、G、L、M 基态原子的最外能层均有2个未成对电子。R+ 核外有 28 个电子。请回答下列问题:(答题时,A、D、E、G、L、M、R 用所对应的元素符号表示)
(1)E、G、M 的第一电离能由大到小的顺序为________。
(2)右图是由 Q、R、G 三种元素组成的一种高温超导体的晶胞结构,其中 R 为+2 价,G 为 -2 价。基态 R2+的核外电子排布式为________;Q的化合价为________。
(3)1 mol 晶体 L 中含有σ键的数目为________。
(4)G与M 可形成 MG3与MG2,MG3分子的空间构型是________,MG2中M原子的杂化方式是________。
(5)在(EA4)2 R(MG4)2 中存在的化学键除极性键外,还有________(填字母)。
a.离子键 b.氢键
c.配位键 d.金属键
查看答案和解析>>
科目: 来源: 题型:
波尔多液是果农常用的一种杀菌剂。氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见下表。
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |
| 白色结晶粉末 | 170~ 172 ℃ | 易溶 于水 |
回答下列问题:
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为________。
(2)氯吡苯脲晶体中,微粒间的作用力类型有________。
A.离子键 B.金属键
C.极性键 D.非极性键
E.配位键 F.氢键
(3)查文献可知,可用2-氯-4-氨吡啶与异氰酸苯酯反应,生成氯吡脲。
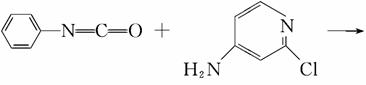
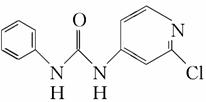
反应过程中,每生成1 mol氯吡苯脲,断裂________个σ键、断裂________个π键。
(4)波尔多液是果农常用的一种杀菌剂,是由硫酸铜和生石灰制得。若在波尔多液的蓝色沉淀上,再喷射氨水,会看到沉淀溶解变成蓝色透明溶液,得到配位数为4的配合物。铜元素基态原子电子排布式为________________。
(5)上述沉淀溶解过程的离子方程式_____________________________
______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下列描述正确的是 ( )。
A.CS2为V形极性分子
B.SiF4与SO 的中心原子均为sp3杂化
的中心原子均为sp3杂化
C.C2H2分子中σ键与π键的数目比为1:1
D.水加热到很高温度都难分解是因水分子间存在氢键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com