
科目: 来源: 题型:
已知某有机物X的结构简式为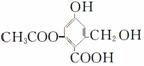 ,下列有关叙述正确的是( )
,下列有关叙述正确的是( )
① 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为 3 mol、4 mol、1 mol
3 mol、4 mol、1 mol
②X在一定条件下能与FeCl3溶液发生显色反应
③X在一定条件下能发生消去反应和酯化反应
④X的化学式为C10H8O6
A.①② B.①③ C.② ④ D.③④
④ D.③④
查看答案和解析>>
科目: 来源: 题型:
一种新型燃 料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷(C2H6)和氧气,其中某一电极反应式为C2H6+18OH--14e-===2CO
料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷(C2H6)和氧气,其中某一电极反应式为C2H6+18OH--14e-===2CO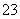 +12H2O。有关此电池的描述不正确的是 ( )
+12H2O。有关此电池的描述不正确的是 ( )
A.通入氧气的电极为正极
B.参加反应的O2与C2H6的物质的量之比为7∶2
C.放电一段时间后,KOH的物质的量浓度将下降
D.放电一段时间后,正极区附近溶液的pH减小
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是( )
A.化学反应达到化学平衡状态的正逆反应速率相等,是指同一物质的消耗速率和生成速率相等,若用不同物质表示时,反应速率不一定相等。
B.标准状况下,1 L辛烷完全燃烧生成CO2 8 L
C.2.4 g Mg无论 与O2还是与N2完全反应,转移电子数都是0.2NA
与O2还是与N2完全反应,转移电子数都是0.2NA
D.1 L 1 mol·L-1 CH3COOH溶液中,所含CH3COO-、CH3COOH的总数为NA
查看答案和解析>>
科目: 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.标准状况下,22.4 L二氯甲烷的分子数约为NA个
B.盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol
C.17.6 g丙烷中所含的极性共价键为4NA个
D.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量一定减少64 g
查看答案和解析>>
科目: 来源: 题型:
下列有关物质性质的说法错误的是( )
A.热稳定性:HCl>HI B.原子半径: Na>Mg
Na>Mg
C.酸性:H2SO3>H2SO4 D.结合质子能力:S2—>Cl—
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式中正确的是( )
A.向碳酸钠溶液中加入足量的盐酸  CO32-+ 2H+ = CO2 ↑+H2O
CO32-+ 2H+ = CO2 ↑+H2O
B.单质铁和三氯化铁溶液反应生成氯化亚铁 Fe + Fe3+=2 Fe2+
Fe2+
C.金属钠与水反应生成氢氧化钠和氢气 Na + H2O=Na++OH-+H2↑
D.氯 化铵晶体和石灰粉共热产生氨气 NH4+ +OH-=NH3↑+H2O
化铵晶体和石灰粉共热产生氨气 NH4+ +OH-=NH3↑+H2O
查看答案和解析>>
科目: 来源: 题型:
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是( )①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转换技术;④田间焚烧秸秆;⑤推广使用节能环保材料。
A.①③⑤ B.②③⑤ C.①②④ D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
 (1)在恒温、恒容容器中发生反应:2SO2 + O2
(1)在恒温、恒容容器中发生反应:2SO2 + O2 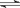 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用O2浓度变化来表示的反应速率为 。如果开始时SO2浓度为4mol/L,O2浓度为2mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 ,达平衡时与反应前压强之比为 。
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用O2浓度变化来表示的反应速率为 。如果开始时SO2浓度为4mol/L,O2浓度为2mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 ,达平衡时与反应前压强之比为 。
(2)右图表示在密闭容器中反应:2SO2+O2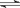 2SO3 △H <0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a 时刻改变条件后达到平衡,新平衡的平衡常数比a时刻前平衡常数 (填“增大”、“减小”或“不变”);b c过程中改变的条件可能是 ; 若增大压强时,反应速率变化情况画在c~d处.
2SO3 △H <0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a 时刻改变条件后达到平衡,新平衡的平衡常数比a时刻前平衡常数 (填“增大”、“减小”或“不变”);b c过程中改变的条件可能是 ; 若增大压强时,反应速率变化情况画在c~d处.
查看答案和解析>>
科目: 来源: 题型:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如右图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com