
科目: 来源: 题型:
利用下列实验装置不能完成相应实验的是 ( )。
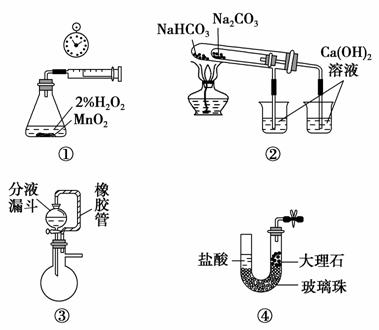
A.用装置①测量生成氧气的化学反应速率
B.用装置②比较NaHCO3和Na2CO3的热稳定性
C.装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶中
D.装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
查看答案和解析>>
科目: 来源: 题型:
按右图装置通入X气体,并在管口P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可能是 ( )。
A.H2和Fe2O3 B.CO和CuO
C.H2和Na2CO3 D.CO和Na2CO3
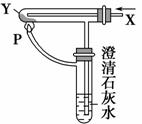
查看答案和解析>>
科目: 来源: 题型:
 用如图所示装置进行下列实验,能达到实验目的的是 ( )。
用如图所示装置进行下列实验,能达到实验目的的是 ( )。
A.瓶中盛有适量浓H2SO4,从A口进气可用来干燥NH3
B.从B口进气,用排空气法收集CO2
C.瓶中盛满水,从B口进气,用排水法收集NO2
D.瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H2的体
积
查看答案和解析>>
科目: 来源: 题型:
苯甲酸广泛用于医药、食品、染料、化工等领域。以下是实验室制备苯甲酸的一种方法。反应原理如下:

 实验步骤:
实验步骤:
下图组装反应装置(冷凝水.夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、9.4g高锰酸钾和3.0mL甲苯。
②将三颈烧瓶中的混合液体搅拌,加热至沸腾,直到甲苯完全反应。
③趁热过滤反应混合物。若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中。
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸。
回答下列问题:
(1)本实验应选择的三颈烧瓶规格为 (填字母序号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)判断甲苯已完全反应的现象是 、回流液不再出现油珠。
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是 ;
苯甲酸粗产品除了可用重结晶法精制外,还可用 法。
A.蒸发 B.升华 C.过滤 D.分液
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100 mL溶液,分别取25.00mL溶液,用0.1000 mo1·L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=24.70mL、V2=24.80 mL、V3= 25.80mL。
①配制溶液时用稀乙醇而不 用蒸馏水作溶剂的原因是 。
用蒸馏水作溶剂的原因是 。
②若用酚酞作指示剂,确定滴定终点 的现象是 。
的现象是 。
③产品的纯度为 。
查看答案和解析>>
科目: 来源: 题型:
由烃A合成有机化合物G(二乙酸乙二酯),采用如图所示的合成路线:

回答下列问题:
⑴已知有机物CH3OOC-COOCH3的名称为乙二酸二甲酯,请写出G的结构简式: 。
⑵在上述反应中属于取 代反应的有 (填序号)。
代反应的有 (填序号)。
⑶E中官能团的名称: 。与A互为同系物的C3H6 分子中最多共面原子有 个 。
。
⑷写出反应④的化学方程式(3分): 。
⑸满足下列条件:①能发生水解反应,②能发生银镜反应,③能 与碳酸氢钠反应的G的同分异构体共有
与碳酸氢钠反应的G的同分异构体共有
(3分)。其中, G的一种同分异体其核磁共振氢谱只有6个峰,面积之比为1:1:1:1:3:3,写 出其结构简式 。
出其结构简式 。
查看答案和解析>>
科目: 来源: 题型:
为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(含Fe2O3.SiO2.Al2O3等)转变成重要的工业原料FeSO4(反应条件略)
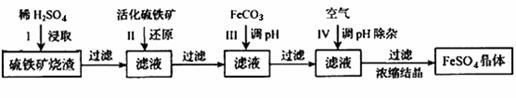
活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2( SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应,请回答下列问题:
SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应,请回答下列问题:
(1)第1步H2SO4与Fe2O3反应的离子方程式是 。
(2)检验第II步中Fe3+是否完全还原,应选择 (填字母编号)。
A.KMnO4溶液 B.K3[Fe(CN)6]溶液 C.KSCN溶液
(3)第III步加FeCO3调溶液pH=6时,利用相关数据计算,判断Al3+是否沉淀完全? (填“是”或“否”)(已知Ksp【Al(OH)3】=1.9×10-33,当离子浓度小于1×10-5mol·L-1时,可认为沉淀完全)
(4)FeCO3在空气中加热反应可制得铁系氧化物材料。
已知25℃,101kPa时:4Fe(s)+3O2(g)=2Fe2O3(s) 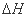 = —1648kJ/mol
= —1648kJ/mol
C(s)+O2(g)=CO2(g) 
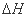 = —393kJ/mol
= —393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) 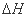
 = —1480kJ/mol
= —1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是 。
(5)FeSO4在一定条件下可制得F eS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li + FeS2 = Fe + 2Li2S,正极反应式是
eS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li + FeS2 = Fe + 2Li2S,正极反应式是 
 。
。
查看答案和解析>>
科目: 来源: 题型:
“低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视。
I. 用电弧法合成的储氢纳米碳管,可用如下氧化法提纯,请完成下述反应:
___  C+ ___ KMnO4 + 6 H2SO4→____CO
C+ ___ KMnO4 + 6 H2SO4→____CO 2↑+ ____MnSO4 + ____K2SO4 + 6 H2
2↑+ ____MnSO4 + ____K2SO4 + 6 H2 O
O
II.某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2 L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,得到如下数据:
CO2(g)+H2(g) △H<0,得到如下数据:
| 实验组 | 温度/℃ | 起始量(mol) | 平衡量(mol) | 达到平衡所 需要时间/min | ||
| CO(g) | H2O(g) | CO2(g) | H2(g) | |||
| I | 800 | 2 | 2 | x | 1 | 5 |
| II | 900 | 1 | 2 | 0.5 | 0.5 | tm |
| III | 900 | 2 | 4 | y | y | tn |
(1)实验I中,前5min的反应速率υ(CO2)= mol•L1•min1。
(2)下列能判断在800℃实验条件下CO(g)与H2O(g)反应一定达到平衡状态的是 。
A.容器内压强不再变化 B.
 C.混合气体密度不变 D.υ正(CO) =
C.混合气体密度不变 D.υ正(CO) = υ逆(CO2)
υ逆(CO2)
(3)实验III中:y= 。
(4)若实验Ⅲ的容器改为在绝热的密闭容器中进行,实验
测得H2O(g)的转化率a(H2O)随时间变化的示意图,
如右图 所示,b点:υ正 υ逆(填“<”.“=”或“>”)。
所示,b点:υ正 υ逆(填“<”.“=”或“>”)。
查看答案和解析>>
科目: 来源: 题型:
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 
 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度.反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度.反应速率分别随时间的变化如下图所示:
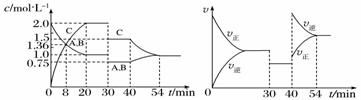
下列说法中正确的是( )
A.30~40 min间该反应使用了催化剂
B.反应方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
下列描述正确的个数是( )
① 聚乳酸的结构为 ,聚乳酸是由单体之间通过加聚而合成
,聚乳酸是由单体之间通过加聚而合成
②完全燃烧 等物质的量的乙醛和乙醇,消耗氧气的质量相等
等物质的量的乙醛和乙醇,消耗氧气的质量相等
③蔗糖.麦芽糖的分子式都是C12H22O11,二者互为同分异构体
④用甘氨酸(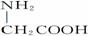 )和丙氨酸(
)和丙氨酸( )缩合最多可形成4种二肽
)缩合最多可形成4种二肽
⑤
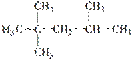 的系统命名法的名称为2,2,3-三甲基戊烷
的系统命名法的名称为2,2,3-三甲基戊烷
A. 1 B.2 C.3 D.4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com