
科目: 来源: 题型:
合金与纯金属制成的金属材料相比,优点是( )
①合金的硬度一般比它的各成分金属的大
②一般地,合金的熔点比它的各成分金属的更低
③改变原料的配比、改变生成合金的条件,得到有不同性能的合金
④合金比纯金属的导电性更强
⑤合金比纯金属的应用范围更广泛
A.②③④ B.①②③⑤
C.①②④ D.①②④⑤
查看答案和解析>>
科目: 来源: 题型:
某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32—、SO32—、SO42—、C1—中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
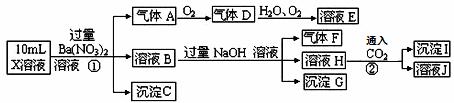
下列说法正确的是( )
A.X中肯定存在Fe2+、NH4+、SO42— B.溶液E和气体F不能发生化学反应
C.X中肯定不存在CO32—、SO32—、C1— D.沉淀I是A1(OH)3
查看答案和解析>>
科目: 来源: 题型:
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g) 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K= | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
| 平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是( )
A.V甲>V丙 B.K乙<K丙 C.c乙>c甲 D.v甲=v丙
查看答案和解析>>
科目: 来源: 题型:
工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分NaClO)。一化学小组在室温下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO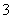 等离子其物质的量(mol)与反应时间t(min)的关系曲线。下列说法错误的是( )
等离子其物质的量(mol)与反应时间t(min)的关系曲线。下列说法错误的是( )
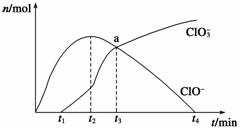
A.工业制取漂白液的化学反应方程式为Cl2+2NaOH===NaCl+NaClO+H2O
B.a点时溶液中各离子浓度:c(Na+)>c(Cl-)>c(ClO3-)=c(ClO-)>c(OH-)>c(H+)
C. t2~t4,ClO-离子的物质的量下降的原因可能是3ClO-= 2Cl-+ClO3-
D.使用漂白液时,为了增强漂白效果,可以向漂白液中加入浓盐酸
查看答案和解析>>
科目: 来源: 题型:
第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态。其电路工作原理如图所示。下列说法中正确的的是( )
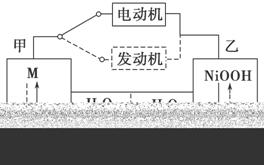
A.电池充电时,OH-由甲侧向乙侧移动
B.甲放电时为正极,充电时为阳极
C.放电时负极的电极反应式为MHn-ne- = M+nH+
D.汽车下坡时发生图中实线所示的过程
查看答案和解析>>
科目: 来源: 题型:
室温下向1L pH=2的醋酸溶液中加入2L pH=2的盐酸,则混合溶液的pH为(假设混合后溶液体积不变,室温下醋酸的电离平衡常数为1.8×10-5)( )
A.2.3 B.1.7 C.2 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
 向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
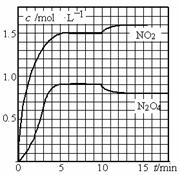
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃, 10min后升高并维持容器的温度为T2℃。下列说法正确的是( )
A.前5min反应的平均速率v(N2O4)=0.18mol·L-1·s-1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2. 0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
科目: 来源: 题型:
下列有关颜色变化错误的是( )
A.在4mL0.1mol/L的K2Cr2O7溶液中滴加数滴1mol/LNaOH溶液,溶液颜色从橙色变成黄色
B.在试管中加入少量氯化钴晶体,滴加浓盐酸溶解后加水稀释至紫色,将试管置于热水中片刻,溶液颜色变成粉红色
C.向血红色的Fe(SCN)3溶液中加入少量KI固体,溶液颜色变浅
D.用50mL针筒抽取30mL红棕色的NO2气体并封住注射孔,当用力推压活塞,压缩针筒中的气体(此过程中不考虑温度变化),从针筒顶端观察,气体颜色逐渐变浅
查看答案和解析>>
科目: 来源: 题型:
下列有关电解质溶液的说法正确的是( )
A.将Ca(ClO)2、Na2SO3、FeCl3溶液蒸干均得不到原溶质
B.保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止Fe2+水解
C.室温下,向0.1mol/L的CH3COOH溶液中加入少量水溶液显碱性的物质,CH3COOH的电离程度一定增大
D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
查看答案和解析>>
科目: 来源: 题型:
现有室温下的四种溶液,其pH如下表所示,下列有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
A.③④中分别加入适量醋酸钠晶体,两溶液pH均增大
B.②③两溶液等体积混合,所得溶液中:c(H+)>c(OH-)
C.分别加水稀释10倍,溶液的pH:①>②>④>③
D.V1L④和V2L①溶液混合后,若pH=7,则V1<V2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com