
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料。下列说法正确的是

A.电极A表面反应之一为NO2-e-+H2O==NO3-+2H+
B.电极B附近的c(NO3-)增大
C.电解质溶液中电流的方向由B到A,电子的流向与之相反
D.该电池工作时,每转移4 mol电子,生成22.4 L O2
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析错误的是
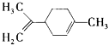
A.在一定条件下,1mol柠檬烯可与2molH2完全加成
B.柠檬烯的一氯代物有7种
C.在一定条件下,柠檬烯可发生加成、取代、氧化、还原反应
D.柠檬烯分子中所有碳原子不可能都在同一平面
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
分子式为C10H14,属于苯的同系物,且苯环上的一氯代物只有2种的有机物有(不考虑立体异构,苯环上至少有3个氢)
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
甲苯是苯的同系物,化学性质与苯相似,但由于基团之间的相互影响,使甲苯的某些性质又与苯不同。下列有关推断及解释都正确的是
A.苯不能通过化学反应使溴水褪色,但甲苯可以,这是甲基对苯环影响的结果
B.苯不能在光照下与Cl2发生取代反应,但甲苯可以,这是苯环对甲基影响的结果
C.苯的一氯代物只有一种,而甲苯的一氯代物有3种,这是苯环对甲基影响的结果
D.苯不能使酸性KMnO4溶液褪色,但甲苯可以,这是苯环对甲基影响的结果
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
0.5mol某烃与1molHCl在一定条件下恰好完全加成,生成物再在光照下与Cl2发生取代反应,氢原子恰好全部被取代消耗Cl2 3mol,则该烃的分子式为
A.C3H6 B.C4H6 C.C3H4 D.C2H4
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)  xC(g) △H>0,其它条件不变,只有温度改变时,某量随温度变化关系如图。则下列说法中错误的是
xC(g) △H>0,其它条件不变,只有温度改变时,某量随温度变化关系如图。则下列说法中错误的是
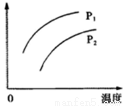
A.纵坐标可能表示C的产率
B.纵坐标一定可以表示混合气体平均摩尔质量
C.若p1>p2,则x=1或2
D.x的取值与p1、p2的相对大小有关
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:填空题
(12分)有机物键线式结构的特点是以线示键,每个折点和线端处表示有一个碳原子,并以氢补足四键,C、H不表示出来,其它原子或原子团要表示出来,例如:CH3CHOHCH3的键线式结构为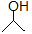 。CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为
。CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为 。
。
(1)CH3CH=CHCH3的名称为 ,其所含官能团的结构式为 ,与H2在一定条件下发生加成反应,其产物的同分异构体的键线式结构为 。
(2)完成下列反应方程式,产物用键线式表示: +Br2→ ,反应类型为 反应。
+Br2→ ,反应类型为 反应。
(3) 是一种加聚产物,则其单体的结构简式为 ,其链节为 。
是一种加聚产物,则其单体的结构简式为 ,其链节为 。
(4)写出与CH3CH=CHCH3含有相同官能团的同分异构体的结构简式 。(任写一种)
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:填空题
(12分)(1)已知反应Ⅰ:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1266.8kJ/mol
反应Ⅱ:N2(g) + O2(g)== 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式 ,该反应的化学平衡常数的表达式K= (用含K1、K2的代数式表示)。
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为: 。该电池使用过程中,正极附近溶液的pH将 (填“升高”、“降低”或“不变”)。
(2)已知:N2(g) +3H2(g)  2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。
①为提高H2的转化率,宜采取的措施有 (填字母)
A.及时移出氨 B.升高温度
C.使用催化剂 D.循环利用和不断补充N2
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为 。
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:填空题
(12分)按要求回答下列问题:
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是 (填字母)
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中不变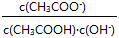
D.溶液中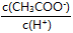 将减小
将减小
E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1:V2= (忽略溶液体积的变化)。
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是 (填字母)
A.若混合后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有:c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c(OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示:
溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①写出向NaClO溶液中通入少量CO2的离子方程式 。
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是 (填字母)
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)= (填准确数值)。
(4)已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于 。
查看答案和解析>>
科目: 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:填空题
(12分)某实验小组的同学对电化学原理进行了一系列探究活动
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示) 设计的原电池装置,反应前,两电极质量相等,一段时间后,两电极质量相差18g,则导线中通过 mol电子。

(2)用胶头滴管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式 ,然后滴加几滴硫氰化钾溶液,溶液变红;继续滴加过量新制饱和氯水,红色褪去,假设之一是“溶液中的+3价铁被氧化为更高的价态”。如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,石墨(1)为 极(填“正”、“负”、“阴”或 “阳”)。在甲装置中滴加几滴酚酞试液,振荡均匀,一段时间后,在甲装置中观察到 电极(填“铁”或“铜”)附近溶液先变红,该电极的反应式为 。
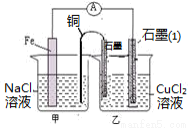
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com