
科目: 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:填空题
(12分) 已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/c2(CH3OH),该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题:
(1)写出上述反应的化学方程式: 。
(2)该反应的△H 0。
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL-1) | 0.54 | 0.68 | 0.68 |
①此时温度400℃,则某时刻υ正 υ逆(填<、>或=,下同)。
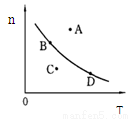
②若以温度为横坐标,以该温度下平衡态甲醇物质的量n为纵坐标,此时反应点在图象的位置是图中 点,比较图中B、D两点所对应的正反应速率υB υD,理由是 。
(4)一定条件下要提高反应物的转化率,可以采用的措施是 。
a.升高温度
b.加入催化剂
c.压缩容器的体积
d.增加水蒸气的浓度
e.及时分离出产物
查看答案和解析>>
科目: 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:填空题
(11分) I:常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表
序号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)根据①组实验情况,分析混合溶液的pH=9的原因是 (用反应的离子方程式表示),在该溶液中下列关系式不正确的是(填序号字母)________。
A.c(Na+)+c(H+)=c(OH-)+c(A-)
B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-)
D.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA)
(2)②组情况表明,c 0.2mol·L-1。混合溶液中离子浓度c(A-) c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明HA的电离程度 NaA的水解程度(选填“>”、“<”或“=”),离子浓度由大到小的顺序是__________________________。
Ⅱ:室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。
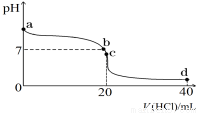
(1)NH3·H2O的电离方程式是 。
(2)b点所示溶液中的溶质是 。
(3)c点所示溶液中,离子浓度从大到小的关系为 。
查看答案和解析>>
科目: 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:填空题
(10分)下图是一个化学过程的示意图。

(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH的电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
A.MgSO4 B.CuSO4 C.NaCl D.CuCl2
查看答案和解析>>
科目: 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:填空题
(12分)(1)某研究性学习小组在实验室中配制1 mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是______________。
A.实验中所用到的滴定管、容量瓶,在使用前均需要检漏;
B.如果实验中需用60 mL 稀硫酸标准溶液,配制时应选用100 mL容量瓶;
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小;
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大;
E.中和滴定时,若在最后一次读数时俯视读数,则导致最后实验结果偏大
(2)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-)/c(H+)=1×10-8。
①常温下,0.1 mol·L-1 HA溶液的pH= ;写出该酸(HA)与NaOH溶液反应的离子方程式: ;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是: ;
③0.2 mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合后所得溶液中:c(H+)+c(HA)-c(OH-)= mol·L-1。(溶液体积变化忽略不计)
(3)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw= 。该温度下(t℃),将100 mL 0.1 mol·L-1的稀H2SO4溶液与100 mL 0.4 mol·L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH= 。
查看答案和解析>>
科目: 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知反应3A(g)+B(g) C(s)+4D(g)+Q,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是
C(s)+4D(g)+Q,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是

①增大B的浓度 ②升高反应温度
③缩小反应容器的体积(加压) ④加入催化剂
A.①② B.①③ C.②③ D.③④
查看答案和解析>>
科目: 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
一定温度下,可逆反应A2(g)+B2(g) 2AB(g)达到平衡状态的标志是
2AB(g)达到平衡状态的标志是
A.单位时间内生成 n mol A2,同时生成 n mol AB
B.体系内的总压不随时间变化
C.单位时间内生成2n mol AB的同时生成n mol B2
D.单位时间内生成 n mol A2的同时,生成n mol B2
查看答案和解析>>
科目: 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是:
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.由H2(g)、I2(g)、HI(g)组成的平衡体系,加压后颜色加深
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目: 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
在2A﹢B 2C﹢D反应中,表示该反应速率最快的是
2C﹢D反应中,表示该反应速率最快的是
A.v(A)=0.8mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.6mol·L-1·s-1 D.v(D)=0.5mol·L-1·s-1
查看答案和解析>>
科目: 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列属于强电解质的是
A.Cu B.CH3COONH4 C.CH3COOH D.NH3·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com