
科目: 来源:2014-2015学年北京市西城区高三二模理综化学试卷(解析版) 题型:实验题
(15分)某小组同学利用铝和氧化铁发生铝热反应后得到的固体进行如下实验。
(1)铝和氧化铁反应的化学方程式是 。
(2)固体成分的初步确定。
实验序号 | 操作及现象 |
ⅰ | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
ⅱ | 向ⅰ中所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液至过量,产生无色气体(经检验为O2),溶液变为深红色,且红色很快褪去 |
①由上述实验可知:溶液中Fe元素的存在形式有 。
②ⅰ中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,设计了相关实验,依据的原理是(用离子方程式表示) 。
③生成O2的化学方程式是 。
进一步的实验表明,上述固体样品中Fe元素的存在形式有:Fe、Fe2O3、Fe3O4。
(3)该小组同学对ⅱ中溶液红色褪去的原因做进一步探究。
实验序号 | 操作、现象 |
ⅲ | 将ⅱ中剩余溶液均分为两份,一份滴加NaOH溶液,产生红褐色沉淀; 另一份滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀不溶解 |
ⅳ | 取2 mL 0.1 mol/L FeCl3溶液,滴入KSCN溶液,溶液变为红色,通入一段时间O2,无明显变化。再加入H2O2溶液,红色很快褪去 |
提示:KSCN中S元素的化合价为-2价
①实验ⅲ中白色沉淀的化学式是 。
②结合实验ⅲ和ⅳ分析,实验ⅱ中红色褪去的原因是 。
③查阅资料得知:Cl-对溶液红色褪去的反应有催化作用,验证该说法应补充的实验和现象是 。
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
化学与环境、生活、材料密切相关。下列说法正确的是
A.安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率
B.二氧化氯和三氯化铁都常用于自来水的处理,二者的作用原理是相同的
C.通过有机合成,可以制造出比钢铁更强韧的新型材料
D.气溶胶和液溶胶的差别在于分散质的物质状态
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
关于过氧化物的叙述正确的是(NA表示阿伏伽德罗常数)
A.7.8 g过氧化钠含有的共用电子对数为0.2NA
B.2H2O2(l)=2H2O(l)+O2(g) ΔH=98.2 kJ·mol1,ΔS=70.5 J·mol1·K1,该反应低温能自发进行
C.过氧化氢使高锰酸钾溶液褪色,1 mol过氧化氢得到2NA电子
D.在含有NH4+ 、Ba2+、Cl—、NO3—离子的溶液 加入少量过氧化钠以上各离子量几乎不减少
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
下表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素。下列说法正确的是
X | ] | |
Y | Z | R |
W |
A.五种元素的原子最外层电子数一定都大于2
B.X、Z原子序数可能相差18
C.Z可能是氯元素
D.Z的氧化物与X单质不可能发生置换反应
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
物质中杂质(括号内为杂质)的检验、除杂的试剂或方法都正确的是
物质及其杂质 | 检验 | 除杂 | |
A | Cl2(HCl) | 湿润的淀粉KI试纸 | 饱和食盐水 |
B | NO(NO2) | 观察颜色或湿润的淀粉KI试纸 | 水 |
C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和Na2CO3溶液 |
D | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
卤素互化物与卤素单质性质相似。已知CH2=CH—CH=CH2(1,3—丁二烯)与氯气发生加成产物有三种:
①CH2Cl—CHCl—CH=CH2 (1,2—加成)
②CH2Cl—CH=CH—CH2Cl (1,4—加成)
③CH2Cl—CHCl—CHCl—CH2Cl(完全加成)
据此推测CH2=C(CH3)—CH=CH2(异戊二烯)与卤素互化物BrCl的加成产物有几种(不考虑顺反异构和镜像异构
A.6种 B.10种 C.12种 D.14种
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
常温下,0.2 mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
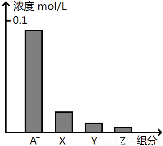
A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
某混合溶液中,含溶质X、Y各0.1 mol,向其中滴加0.1 mol/L的Z溶液,所得沉淀的物质的量如下图,则符合条件的X、Y、Z分别是
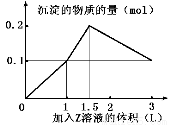
A.氯化铝、 氯化铁、 氢氧化钠
B.氯化铝、 氯化镁、 氢氧化钠
C.偏铝酸钠、 氯化钡、 硫酸
D.偏铝酸钠、 氢氧化钡、 硫酸
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:实验题
(14分)铝热反应是铝的一个重要性质。某校化学兴趣小组同学,取磁性氧化铁在如图实验装置进行铝热反应,冷却后得到“铁块”混合物。

(1)取反应后的“铁块”研碎取样称量,加入如图装置滴入足量NaOH溶液充分反应,测量生成气体体积。试回答下列问题:
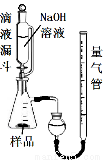
①该实验的实验目的是:测量样品中 的百分含量(填物质名称)。
②量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为 。
③量气管在读数时调节左右管液面相平之前的步骤是________ _。
④装置中使用带平衡管的滴液漏斗代替普通分液漏斗,除了可以平衡压强让液体顺利滴入锥形瓶之外还可以起到降低实验误差的作用。如果装置使用分液漏斗,测量出的该物质百分含量将会 (填“偏大”或“偏小”)。
(2)另称取“铁块”样品溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。为测定该实验所得 “铁块”的成分,实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
①试剂A应选择 ,试剂B应选择 。(填序号)
A.稀盐酸
B.氧化铁
C.H2O2溶液
D.氨水
E.MgCO3固体
②灼烧完全的标志是 。
③若最终红色粉未M的质量为12.0 g,则该“铁块”中铁的百分含量是 。
查看答案和解析>>
科目: 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:实验题
(15分)高锰酸钾[KMnO4]是常用的氧化剂。工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。中间产物为锰酸钾[K2MnO4]。下图是实验室模拟制备的操作流程:
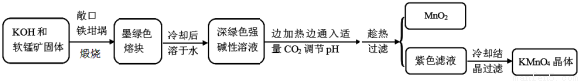
相关资料:
①物质溶解度
物质 | KMnO4 | K2CO3 | KHCO3网] | K2SO4 | CH3COOK |
20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶。其水溶液呈深绿色,这是锰酸根(MnO42—)的特征颜色。
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42—会发生歧化反应。
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;
实验中用铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为_______。
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低。请写出实验中通入适量CO2时体系中可能发生反应离子方程式 : ;
其中氧化还原反应中氧化剂和还原剂的质量比为_________________________。
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸。从理论上分析,选用下列酸中________ ,得到的产品纯度更高。
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程为_________;
传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低。有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图)。
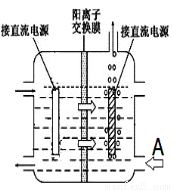
图中A口加入的溶液最好为__________。
使用阳离子交换膜可以提高Mn元素利用率的原因为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com