
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列说法正确的是
A.在反应中消耗0.1molCl2,转移的电子数一定为0.2NA
B.15gCH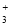 (碳正离子)中含有的电子数为10NA
(碳正离子)中含有的电子数为10NA
C.标准状况下,0.5mol氦气含有的电子数为NA
D.0.1L 2mol·L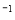 的(NH4)2S溶液中含有的S
的(NH4)2S溶液中含有的S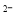 数目为0.2 NA
数目为0.2 NA
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是
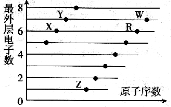
A.ZY、ZW的水溶液都显酸性
B.原子半径大小:W>R>X,离子半径大小:Z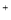 >R
>R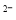 >W
>W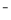 >Y
>Y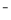
C.W的氢化物水溶液的酸性比R的氢化物水溶液的酸性强,可证明非金属性:W>R
D.Z、X两种元素可形成的Z2X、Z2X2、ZX2等多种离子化合物
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
某学生以铁丝和Cl2为原料进行下列三个实验。
从分类角度下列分析正确的是
A.实验①、③反应制得的物质均为纯净物
B.实验②、③均未发生氧化还原反应
C.实验②、③均为放热反应
D.实验①、②所涉及的物质均为电解质或非电解质
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验。羟基硝酸铵的结构如图所示,下列说法不正确的是
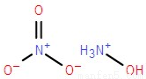
A.羟基硝酸铵中阳离子的各原子共平面
B.羟基硝酸铵是离子化合物
C.羟基硝酸铵中含有离子键和共价键
D.9.6g羟基硝酸铵中含有0.2mol离子
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
[Fe(CN)6]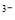 可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为[Fe(CN)6]
可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为[Fe(CN)6]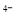 。工业上常采用如图所示的电解装置,通电电解,然后通入H2S加以处理。下列说法不正确的是
。工业上常采用如图所示的电解装置,通电电解,然后通入H2S加以处理。下列说法不正确的是
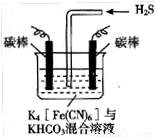
A.电解时阳极反应式为[Fe(CN)6]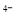 -e
-e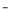
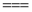 [Fe(CN)6]
[Fe(CN)6]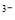
B.电解时阴极反应式为+2 e
 H2
H2 +2CO
+2CO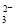
C.当电解过程中有22.4L标准状况下的H2生成时,溶液中有32gS析出(溶解忽略不计)
D.整个过程中需要不断补充K4 [Fe(CN)6]与KHCO3
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是
A.钠在氧气中燃烧,钠的氧化产物: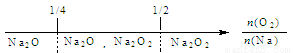
B.铁在Cl2中燃烧,铁的氧化产物: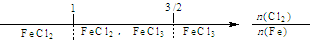
C.NH3与Cl2反应,反应产物: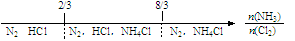
D.FeBr2溶液中通入Cl2,铁元素存在形式:
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:简答题
(13分)1902年德国化学家哈博研究出合成氨的方法,其反应原理为:
N2(g)+3H2(g)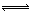 2NH3(g); △H(△H<0)
2NH3(g); △H(△H<0)
一种工业合成氨的简易流程图如下:
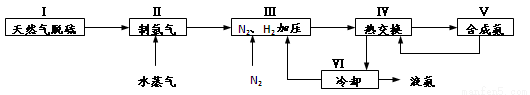
完成下列填空:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生。NH4HS的电子式是___________,写出再生反应的化学方程式:__________________。NH3的沸点高于H2S,是因为NH3分子之间存在着一种比_________力更强的作用力。
(2)室温下,0.1 mol/L的氯化铵溶液和0.1 mol/L的硫酸氢铵溶液,酸性更强的是_______,其原因是___________________________________________________________。
已知:H2SO4:H2SO4 = H++HSO4-;
HSO4-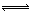 H++SO42- :
H++SO42- :
K =1.2×10-2 NH3·H2O:K=1.8×10-5
(3)图甲表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:______(保留3位有效数字)。
(4)依据温度对合成氨反应的影响,在图乙坐标系中,画出一定条件下的密闭容器内,从常温下通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。


(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)________。
简述本流程中提高合成氨原料总转化率的方法(只答一种即可):_________________。
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:简答题
(15分)(NH4)2Fe(SO4)2俗称莫尔盐,其常见的制备工艺流程如下:
(1)已知流程中铁粉制备反应如下:
4 H2O(g) +3Fe(s) Fe3O4(s)十4H2(g) △H =a kJ /mol
Fe3O4(s)十4H2(g) △H =a kJ /mol
Fe3O4(s) = 3 Fe(s)+ 2O2(g) △H =b kJ/mol
则光解气态水制备H2的热化学方程式为 。
(2)步骤I中加水发生如下反应,请完善该反应: +2H2O  2H++ H2TiO3 ↓;
2H++ H2TiO3 ↓;
该步骤加入铁粉的作用是① ;② 。
(3)步骤Ⅳ生成(NH4)2Fe(SO4)2,其化学反应方程式为 ;
写出(NH4)2Fe(SO4)2溶液中各离子溶度由大到小的顺序:
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化。据此分析(NH4)2Fe(SO4)2比FeSO4稳定的原因是 。
(5)室温时Fe(OH)3的悬浊液中存在Fe(OH)3(s) Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)=0.08 mol·L-1则溶液的pH等于 。
Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)=0.08 mol·L-1则溶液的pH等于 。
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:实验题
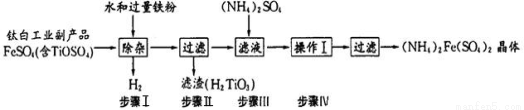
(15分)已知铁离子,氯气、溴均为常见的氧化剂,某化学兴趣小组设计了如下实验探究其强弱:
(1)①装置A中发生反应的离子方程式是 。
②整套实验装置存在一处明显的不足,请指出 。
(2)用改正后的装置进行实验,实验过程如下:
实验操作 | 实验现象 | 结论 |
打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后 。 (填具体实验操作) | D装置中:溶液变红 E装置中:水层溶液变黄, 振荡后,下层CCl4层无明显变化。一段时间后 。(填实验现象) | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: Cl2 >Br2 >Fe3+ |
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化。
D装置中:红色慢慢褪去。
E装置中:CCl4层颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
ⅰ.Fe3+ +3SCN- ⅱ.(SCN)2性质与卤素单质类似。氧化性:Cl2 > (SCN)2 。 |
①请用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因 。
现设计简单实验证明上述解释:取少量褪色后的溶液,滴加 溶液,若溶液颜色 。则上述解释是合理的。
小组同学另查得资料如下:
ⅲ.Cl2和Br2反应生成BrCl,BrCl呈红色(略带黄色),沸点约5℃,它与水能发生水解反应,且该反应为非氧化还原反应。 ⅳ.AgClO、AgBrO均可溶于水。 |
②欲探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步离子方程式解释仅产生白色沉淀原因 、 。
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:简答题
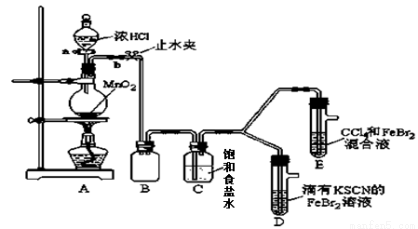
【化学─选修2:化学与技术】(15分)硫酸工业的废渣回收再利用的工艺流程如下:
注:硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,② 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为 。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:
准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-,
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓,
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O。
①若SnCl2不足量,则测定的Fe3+量 (填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量 。
(4)①可选用 (填试剂)检验滤液中含有Fe3+。“酸浸”后Fe2+可被空气中O2氧化(用离子反应方程式表示) 。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
第一步:氧化: ;(填写具体操作)
第二步:沉淀 ;(填写具体操作)
第三步:分离,洗涤;
第四步:烘干,研磨。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com