
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:选择题
下图为某化学课外学习小组设计的电解饱和食盐水的简易装置。下列有关说法正确的是

A.电解一段时间后,往蛋壳中溶液中滴加几滴酚酞,呈红色
B.蛋壳表面缠绕的铁丝发生氧化反应
C.铁丝表面生成的气体能使湿润的淀粉碘化钾试纸变蓝
D.蛋壳可阻止生成的氯气与氢气、氢氧化钠溶液接触
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:选择题
常温下,0.1mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是
A.该溶液中由水电离出的c(H+)=1×10-3 mol·L-1
B.由pH=3的HA溶液与pH=11的NaOH溶液等体积混合,则该混合溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C.浓度均为0.1mol/L的HA和NaA溶液等体积混合。若该混合溶液呈酸性,则c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
D.0.1mol·L-1的HA溶液与0.05mol·L-1的NaOH溶液等体积混合,则其所得溶液中2c(H+)+c(HA)=c(A-)+2c(OH-)
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:实验题
(12分)实验室里用加热正丁醇、溴化钠和浓硫酸的混合物的方法来制备1—溴丁烷时,还会有溴、烯和醚等产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷。已知有关物质的性质如下:
熔点/℃ | 沸点/℃ | 密度/g·cm-3 | |
正丁醇 | -89.53 | 117.25 | 0.81 |
1—溴丁烷 | -112.4 | 101.6 | 1.28 |
丁醚 | 95.3 | 142 | 0.76 |
1—丁烯 | -185.3 | -6.5 | 0.59 |

(1)生成1—溴丁烷的反应装置应选用上图中的 (填序号),反应加热时温度t1应控制在 100℃。
(2)生成1—溴丁烷的化学方程式为 。
(3)反应中由于发生副反应而生成副产物的反应类型依次有(按生成溴、烯、醚的先后顺序) 。
(4)反应结束后,将反应混合物中1—溴丁烷分离出,应采用方法是 ,该操作应控制温度t2的范围是 。
(5)在最后得到的1—溴丁烷的产物中,可能含有的杂质主要是 ,进一步除去的方法是 。
(6)在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,欲知哪一层液体是“水层”,其简便的判断方法是 。
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:填空题
(15分)蛇文石矿可以看作是由MgO、Fe2O3、Al2O3、SiO2组成。由蛇文石制取碱式碳酸镁的实验步骤如下:
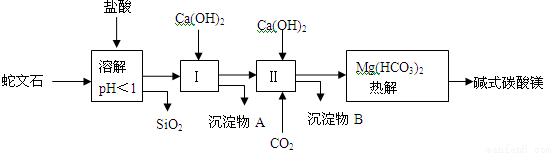
(1)蛇文石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是 。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.3 | 9.6 |
Ca(OH)2不能过量,若Ca(OH)2过量会导致 溶解、生成 沉淀。
(3)从沉淀混合物A中提取红色氧化物做颜料,先向沉淀物A中加入 (填物质的化学式),然后 (依次填写实验操作名称)。
(4)物质循环使用可节约能源。上述实验中,可以循环使用的物质是 (填写物质的名称)。
(5)设计一个实验,确定产品a MgCO3·b Mg(OH)2·cH2O中的a、b、c的值。将32.8g产品完全分解后,产生13.2g CO2和16.0g MgO。由此可知,产品的化学式中a∶b∶c= 。(填最简整数比)
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:简答题
(16分)二氧化碳被认为是加剧温室效应的主要来源。2014年11月12日中美两国在北
京发表《中美气候变化联合声明》,中国政府承诺到2030年前停止增加二氧化碳排放,
为此政府大力推广二氧化碳的综合开发和利用。以CO2和NH3为原料合成尿素是固定和
利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s) △H1 = a kJ·mol-1
NH2CO2NH4(s) △H1 = a kJ·mol-1
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) △H2 =+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2 =+72.49kJ·mol-1
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H3 =-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g) △H3 =-86.98kJ·mol-1
请回答下列问题:
(1)反应Ⅰ的△H1 =__________kJ·mol-1(用具体数据表示)。
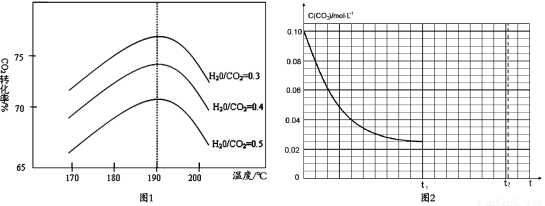
(2)反应Ⅲ中影响CO2平衡转化率的因素很多,图1为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2平衡转化率变化的趋势曲线。
①其他条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是_________(填“提高”或“降低”)水碳比。
②当温度高于190℃后,CO2平衡转化率出现如图1所示的变化趋势,其原因是__________________。
(3)反应Ⅰ的平衡常数表达式K1 =____________________。
(4)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,从反应开始到达到平衡过程中c(CO2)随时间t变化趋势的曲线如图2所示。若其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)。
(5)尿素在土壤中会发生反应CO(NH2)2+2H2O (NH4)2CO3。下列物质中与尿素有类似性质的是______。
(NH4)2CO3。下列物质中与尿素有类似性质的是______。
A.NH2COONH4
B.H2NOCCH2CH2CONH2
C.HOCH2CH2OH
D.HOCH2CH2NH2
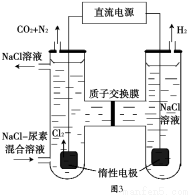
(6)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图3。阳极室中发生的反应为 、 。
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:简答题
【化学—选修2:化学与技术】(15分)重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3,杂质为SiO2、Al2O3)为原料生产它,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下图。涉及的主要反应是6FeO·Cr2O3+24NaOH+7KClO3=12Na2CrO4+3Fe2O3+7KCl+12H2O
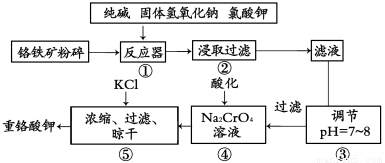
(1)碱浸前将铬铁矿粉碎的作用是 。
(2)步骤③调节pH后过滤得到的滤渣是 。
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式 。
(4)用简要的文字说明操作⑤加入KC1的原因 。
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I一十S4O52-)
①判断达到滴定终点的依据是 。
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度为(设整个过程中其它杂质不参加反应) (保留2位有效数字)。
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】(15分)已知位于元素周期表前四周期的六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成A2C型离子化和物,其中的阴、阳离子相差一个电子层,E4+离子和氩原子的核外电子排布相同。请回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序是____________(填元素符号)
(2)化合物BD3的分子空间构型可描述为_________,B的原子轨道杂化类型为_______。
(3)已知F元素在人体内含量偏低时,会影响O2在体内的正常运输。已知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物。则F的基态原子价电子排布式为________________。CN-与___________(一种分子)互为等电子体,则1个CN-中π键数目为___________。
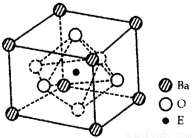
(4)EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为__________
在该晶体中,E4+的氧配为数为___________。若该晶胞边长为a nm可计算该晶体的密度为__________g/cm3(阿伏加德罗常数为NA)
查看答案和解析>>
科目: 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】(15分)某抗结肠炎药物有效成分及有机化工原料L(分子式为C16H14)的合成路线如下(部分反应略去试剂和条件):
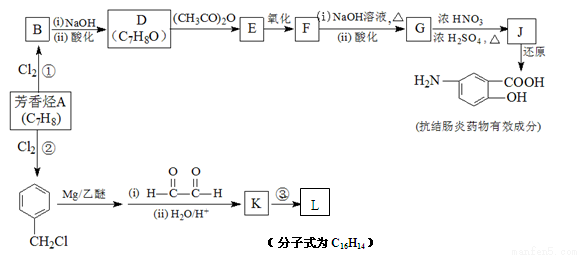
已知:
Ⅰ.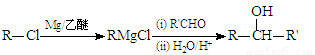 (R、R`表示烃基)
(R、R`表示烃基)
Ⅱ.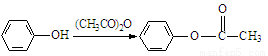
(1)抗结肠炎药物有效成分分子中能与H+反应的官能团名称是 。
(2)B的名称是 ;②中的反应条件是 ;G生成J的反应类型是 。
(3)①的化学方程式是 。
(4)F的结构简式是 。
(5)③的化学方程式是 。
(6)设计D→E和F→G两步反应的目的是 。
(7)已知L有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式。
a.结构中有两个苯环,无其它环状结构
b.苯环上的一硝基取代产物有两种
查看答案和解析>>
科目: 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
化学与科技、生产、生活密切相关。下列说法正确的是
A.气象环境报告中的“PM2.5”是一种新分子的描述
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量、
C.“玉兔号”月球车太阳能电池帆板的材料是二氧化硅
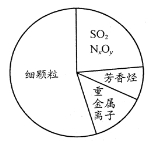
D.上图为雾霾的主要成分示意图,SO2和NxOy都属于酸性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com