
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:选择题
短周期元素甲、乙、丙、丁的原子序数依次增大,甲位于第VA族,乙原子的核外电子数比甲原子多1,乙与丁同族,丙原子最外层电子数与电子层数相等。下列判断正确的是
A.原子半径:丁>丙>乙
B.甲的气态氢化物的水溶液呈酸性
C.乙与丙形成的化合物既能与酸反应,又能与碱反应
D.同周期元素中丁的最高价氧化物对应水化物的酸性最强
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:选择题
将5.4g Al投入200.0mL 2.0mol·L-1的某溶液中有H2产生,充分反应后有金属剩余。该溶液可能为
A.HNO3溶液 B.NaOH溶液 C.H2SO4溶液 D.盐酸
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:选择题
对乙烯基苯甲酸在医药中间体合成中有着广泛的用途,可用化合物M反应合成。下列关于化合物M和对乙烯基苯甲酸的说法正确的是
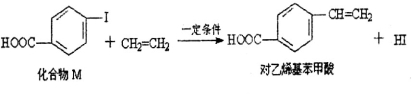
A.对乙烯基苯甲酸的分子式为C9H10O2
B.对乙烯基苯甲酸的同分异构体共有三种
C.对乙烯基苯甲酸即属于羧酸,又属于烯烃
D.二者均可发生取代反应和聚合反应
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:选择题
下列关于实验的描述错误的是
A.将硫酸铜溶液加热蒸发、浓缩、冷却结晶,可以制备硫酸铜晶体
B.测定等浓度NaClO溶液和Na2SO4溶液的pH,比较Cl、S元素的非金属性强弱
C.萃取法除去NaBr溶液中的少量NaI,需要用烧杯、玻璃棒、胶头滴管、分液漏斗
D.检验Na2SO3固体是否被部分氧化:取少量固体溶于水,滴加过量稀盐酸,观察是否产生气泡,再滴加BaCl2溶液,观察是否产生白色沉淀
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:选择题
下列叙述或解释事实的方程式错误的是
A.pH=1的NaHSO4溶液中:c(H+)=c(SO42-)+c(OH—)
B.0.1 mol·L-1 CH3COOH溶液的pH>1:CH3COOH CH3COO—+H+
CH3COO—+H+
C.用NaHCO3溶液做导电实验,灯泡发光:NaHCO3 =Na++H++CO32-。
D.盛满NO2的烧瓶浸泡在冷水中,颜色变浅:NO2 (g,红棕色) N2O4(g,无色)△H<0
N2O4(g,无色)△H<0
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:选择题
饱和氯水中存在平衡:①C12+H2O H++Cl—+HClO,②HClO
H++Cl—+HClO,②HClO H++ClO—,取饱和氯水分别进行下列实验,相应结论错误的是
H++ClO—,取饱和氯水分别进行下列实验,相应结论错误的是
A.逐滴加入氨水中,所得溶液中c(H+)逐渐增大
B.继续通入过量C12,①、②均向右移动,溶液pH减小
C.加入CaCO3悬浊液中,CaCO3的溶解平衡向右移动
D.加入一定量NaOH溶液中,所得溶液中离子浓度的关系可能为c(Cl-)+ c(ClO-)= c(Na+)
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:简答题
(17分)运用化学反应原理研究碳、氮、硫元素及其化合物有重要意义。
(1)已知一定量的C单质能在O2(g)中燃烧,其可能的产物及能量关系如图所示:
写出CO2(g)与C(s)反应生成CO(g)的热化学方程式_______________________。
(2)汽车尾气净化过程中发生反应2NO(g)+2CO(g) N2+2CO2(g) △H<0。一定条件下,向某密闭恒容容器中按体积比1:l充入44.8L(标准状况)NO和CO混合气体,发生上述反应,某同学根据反应过程中的有关数据绘制了如图所示曲线。
N2+2CO2(g) △H<0。一定条件下,向某密闭恒容容器中按体积比1:l充入44.8L(标准状况)NO和CO混合气体,发生上述反应,某同学根据反应过程中的有关数据绘制了如图所示曲线。
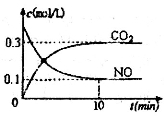
①下列关于上述反应过程的叙述正确的是 ________(填写字母代号)。
A.其它条件不变,加入催化剂,△H的值不变
B.及时除去二氧化碳,反应的正反应速率加快
C.NO、CO、N2、CO2浓度均不再变化,说明平衡未发生移动
D.混合气体的平均相对分子质量不再改变,证明反应达到化学平衡状态
②前10min内CO的平均反应速率为______,达平衡时NO的转化率为_____,能使上述平衡体系中 增大的措施有__________(任写一条)。
增大的措施有__________(任写一条)。
(3)已知弱电解质在水中的电离平衡常数(25℃)如下表(单位省略):
弱电解质 | H2CO3 | H2SO3 | NH3·H2O |
电离平衡常数 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 | Kb=1.7×10-5 |
①室温条件下。用敞口容器加热氨水一段时间,恢复至室温后,溶液中水的电离程度比加热前_______(填写“增大”、“减小”或“不变”)了.
②常温下,0.1 mo1·L-1(NH4)2SO4溶液呈_____(填“酸”、“中”、“碱”)性。
③常温下,测得某碳酸饮料的pH=6,则该饮料 ________。
________。
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:填空题
(16分)金属铝、铁、铜及其化合物与生产、科研关系密切。
(1)工业上可用铝与软锰矿(主要成分为MnO2)反应冶炼金属锰。用化学方程式表示其冶炼原理________。
(2)工业上,采用石墨、铁棒作为电极,电解除去废水中的CN—(C为+4价。下同),装置如图所示,通电过程中,阴、阳两极均有无色无味的气体产生,阳极区两种离子的放电产物会进一步发生反应,其方程式为C12+CNO—+OH— →□+Cl—+CO32-+H2O(未配平)。

①铁电极应连接直流电源的________________(填写电极名称)。
②上述反应方程式配平后“□”内应填写_______。
③阴极产物有______,阳极上发生的电极反应为2Cl--2e-=Cl2↑和______。
(3)用CuSO4溶液为电解质溶液,进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼。下列说法错误的是___________(填写字母代号)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(4)硫酸铝铵水溶液呈酸性,是因为________(填写离子符号)发生了水解;常温下浓度均为0.1 mol·L-1硫酸铝和硫酸铝铵两种水溶液,c(Al3+)较大的是________(填“硫酸铝铵”或“硫酸铝”)溶液。
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:实验题
(20分)某兴趣小组设计如图装置制取SO2,研究其性质,并进一步探究在适当温度和催化剂的条件下,SO2与O2反应后混合气体的成分。
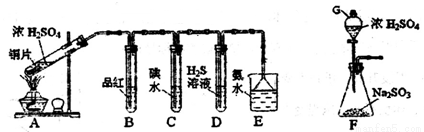
(1)仪器G的名称是_________________。
(2)B、C、D分别用于检验SO2的漂白性、还原性和氧化性。则C中反应的离子方程式为_____________,证明SO2有氧化性的实验现象是___________________.
(3)为了实现绿色环保的目标,某同学设计装置F来代替装置A。与装置A相比,装置F的优点是____________________________(写出2点)。
(4)若选用装置F制取O2,可选用试剂_______________。
(5)该小组同学设计如下装置来检验SO2与O2反应后混合气体的成分。
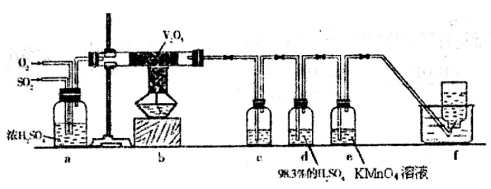
已知:SO3遇水剧烈反应,放出大量热。产生酸雾;98.3%的H2SO4可以吸收SO3和酸雾。
供选试剂:蒸馏水、0.5 mol·L-1BaCl2溶液、98.3%的H2SO4、2.0 mol·L-1 NaOH溶液、KMnO4溶液。
①c中应选用的试剂是_________,e中试剂的作用是__________,f中收集的气体是____________。
②某同学提出用饱和NaHSO3溶液代替98.3%的H2SO4,请你评价该方案是否可行,若可以不必说明理由:若不可行。简述其理由__________。
查看答案和解析>>
科目: 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:填空题
选做(12分)【化学—物质结构与性质】N和B元素在化学中占有很重要的地位。
(1)写出N元素基态原子的价电子排布式_______。B、N和O元素的电负性由大到小的顺序为_______.
(2)N和B两元素氟化物的化学式相似,均为AB3型,但分子的空间结构有很大不同,其原因是___________,其中BF3的分子构型为_______________。
(3)BN的晶体结构与金刚石相似其中B原子的杂化方式为_______,微粒间存在的作用力是_________。
(4)根据电子云的重叠方式判断,N2分子中存在的σ键和π键数目之比为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com