
科目: 来源: 题型:
下列对难溶电解质的溶解平衡的叙述,错误的是
A.难溶电解质的溶解平衡是一种动态平衡
B.达到溶解平衡时,沉淀的速率和溶解的速率相等,溶液中离子的浓度保持不变
C.达到溶解平衡时,溶液中各种离子的浓度不一定相等
D.达到溶解平衡时,再加入该难溶电解质,将促进其溶解
查看答案和解析>>
科目: 来源: 题型:
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题
(1)肼燃料电池原理如图1所示,左边电极上发生的电极反应式为 .
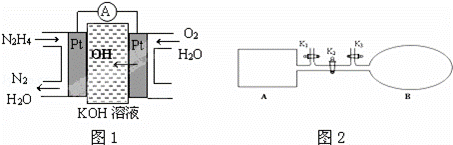
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
N2(g)+2O2(g)=2NO2(g)△H=﹣67.7kJ•mol﹣1
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534.0kJ•mol﹣1
2NO2(g)⇌N2O4(g)△H=﹣52.7kJ•mol﹣1
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式: .
(3)如图2所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L.
①B中可通过 判断可逆反应2NO2⇌N2O4已经达到平衡.
②若打开K2,平衡后B容器的体积缩至0.4a L,则打开K2之前,气球B体积为 L.
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E五种溶液分别是NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
①将1L pH=3的A溶液分别与0.001mol/L x L B溶液、0.001mol/L y L D溶液充分反应至中性,x、y的大小关系式y<x;
②浓度均为0.1mol/L A和E溶液,pH:A<E
③浓度均为0.1mol/L C和D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)C是 溶液,D是 溶液.
(2)用水稀释0.1mol/L B溶液时,溶液中随水量的增加而减小的是 .
A.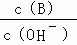 B.
B.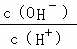 C.c (H+)•c (OH﹣) D.n (OH﹣)
C.c (H+)•c (OH﹣) D.n (OH﹣)
(3)等pH、等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出的氢气的质量相同.则 (填化学式)溶液中锌粉有剩余.
(4)常温下,向0.01mol/L C溶液中滴加0.01mol/L D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为 .
(5)已知常温下Mg(OH)2在pH=12的D溶液中Mg2+的浓度为1.8×10﹣7mol/L,则 Ksp[Mg(OH)2]= .
查看答案和解析>>
科目: 来源: 题型:
短周期元素 X、Y、Z 可组成化学式为 XYZ3 的四种化合物甲、乙、丙、丁.
(l)若甲中 X 的原子只有一个质子,Y、Z同周期,画出Z的电子排布图为 .
(2)若乙中X、Y、Z 三种元素的原子序数之和为 26,Y、Z 同周期,且乙是一种微溶于水的盐,并写出工业制备单质X的化学方程式: .
(3)若丙中X元素的焰色反应为黄色,Y与X同周期,Y 是同周期中原子半径最小的元素,丙与浓盐酸反应生成 Y 单质的化学方程式为 .
(4)若丁中 X、Y、Z 处于不同周期,X的族序数是周期序数的二倍,Z原子核外电子占有9个轨道,且具有一个未成对电子,则丁的结构式为 .
查看答案和解析>>
科目: 来源: 题型:
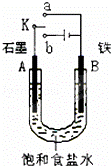
某课外活动小组同学用如图装置进行实验,试回答下列问题.
(1)若开始时开关K与a连接,则B极的电极反应式为 .有关该实验,下列说法正确的是(填序号) .
①A为正极,B为负极
②电子由电极B流出经溶液流向A极
③溶液中Na+向A极移动
④该反应相当于在模拟钢铁的析氢腐蚀
(2)若开关K与b连接,则可模拟工业上离子交换膜法制烧碱,该电池的总反应可表示为(离子方程式) .
有关该实验,下列说法正确的是(填序号) .
①B为阴极,发生氧化反应
②A极电极反应式可表示为2Cl﹣=Cl2↑+2e﹣
③溶液中Na+向A极移动
④若标准状况下B极产生2.24L气体,则电路中通过的电子数为0.2NA.
查看答案和解析>>
科目: 来源: 题型:
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)⇌CO2+H2(g)反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
依据题意回答下列问题:
(1)反应在t1min内的平均速率为v(H2)= mol•L﹣1•min﹣1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2O,到达平衡时,n(CO2)= mol.
(3)保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率 (填“增大”或“减小”或“不变”),H2O的体积分数 (填“增大”或“减小”或“不变”).
(4)温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”).
查看答案和解析>>
科目: 来源: 题型:
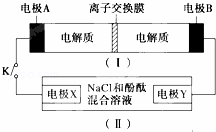
如图装置Ⅰ为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3 K2S2+3KI装置Ⅱ为电解池的示意图.当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
K2S2+3KI装置Ⅱ为电解池的示意图.当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
|
| A. | K+从右到左通过离子交换膜 |
|
| B. | 电极A的反应式:I3﹣+2e﹣=3I﹣ |
|
| C. | 电极X的反应式:4OH﹣﹣4e﹣═O2↑+2H2O |
|
| D. | 当电极Y有0.2mole﹣转移时,产生0.1molCl2 |
查看答案和解析>>
科目: 来源: 题型:
下列各组离子在指定的溶液中能大量共存的是( )
①无色溶液中:K+、Cu2+、Na+、SO42﹣
②常温下pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣
③加入Al能放出H2的溶液中:Cl﹣、HCO3﹣、NO3﹣、NH4+
④在由水电离出的c(OH﹣)=10﹣13 mol•L﹣1的溶液中:Na+、Ba2+、Cl﹣、I﹣
⑤能使红色石蕊试纸变为蓝色的溶液:Na+、Al3+、Cl﹣、S2﹣
⑥使pH试纸呈红色的溶液中:Fe2+、Al3+、NO3﹣、Cl﹣.
|
| A. | ②④ | B. | ③⑤ | C. | ④⑥ | D. | ②⑤ |
查看答案和解析>>
科目: 来源: 题型:
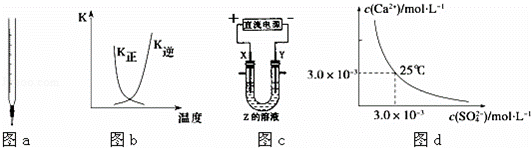
下列图示与对应的叙述相符的是( )
|
| A. | 图a为碱式滴定管,可盛装NaOH、KMnO4等溶液,不可盛装酸性液体 |
|
| B. | 图b中曲线表示反应2A(g)+B(g)⇌2C(g)△H>0,正、逆反应的平衡常数K随温度的变化 |
|
| C. | 图c表示铜的精炼,则X是精铜,Y是粗铜,Z是CuSO4溶液 |
|
| D. | 图d表示25℃时,CaSO4在水中的沉淀溶解平衡曲线.向100 mL该条件下的CaSO4饱和溶液中加入100 mL 0.01mol•L﹣1的Na2SO4溶液有沉淀析出 |
查看答案和解析>>
科目: 来源: 题型:
下列有关金属腐蚀与防护的说法正确的是( )
|
| A. | 纯银器表面在空气中因电化学腐蚀渐渐变暗 |
|
| B. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
|
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
|
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com