
科目: 来源: 题型:
在密闭容器中发生如下反应:mA(g)+nB(g)⇌pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的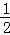 ,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是()
,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是()
A. m+n>p B. 平衡向逆反应方向移动
C. A的转化率提高 D. C的体积分数增加
查看答案和解析>>
科目: 来源: 题型:
已知反应A2(g)+2B2(g)⇌2AB2(g)△H<0,下列说法正确的是()
A. 升高温度,正反应速率增大,逆反应速率减小
B. 增大压强可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
C. 达到平衡后,升高温度或减小压强平衡都向逆反应方向移动
D. 使用催化剂,可以改变活化能,从而改变反应的△H
查看答案和解析>>
科目: 来源: 题型:
下列说法或描述中,不符合实际的是()
A. 医用药品应在低温、干燥的环境下密封保存
B. 反应中的某一物质的转化率α(B)增大,则该反应的平衡常数K一定增大
C. 向一堆篝火“鼓风”,有助于它继续燃烧下去
D. 微量的MnO2粉末可以使过氧化氢快速分解,而MnO2的质量在反应前后并没发生变化
查看答案和解析>>
科目: 来源: 题型:
模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g)⇌H2(g)+Br2(g)反应.下列四个图中可以表示该反应在一定条件下为可逆反应的是()
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目: 来源: 题型:
传统合成氨工业需要采用高温、高压和催化剂.近来美国化学家使用新型铁系催化剂,在常温下合成了氨气.下列说法正确的是()
A. 新型合成氨方法是吸热反应
B. 新型合成氨方法可简化生产设备
C. 新型催化剂提高了N2和H2的转化率
D. 两种方法中该反应的化学平衡常数相同
查看答案和解析>>
科目: 来源: 题型:
下列有关能量转换的说法正确的是()
A. 煤燃烧是化学能转化为热能的过程
B. 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C. 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D. 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
查看答案和解析>>
科目: 来源: 题型:
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g),随温度的升高,混合气体的颜色变深.
回答下列问题:
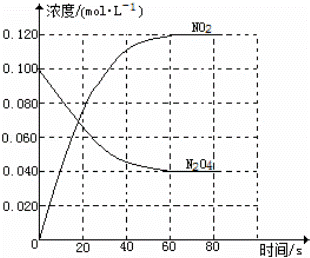
(1)反应的△H 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为 mol•L﹣1•s﹣1;反应的平衡常数K1为 .
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol•L﹣1•s﹣1的平均速率降低,经10s又达到平衡.
①T 100℃(填“大于”或“小于”),判断理由是 .
②列式计算温度T时反应的平衡常数K2 .
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反应”)方向移动,判断理由是 .
查看答案和解析>>
科目: 来源: 题型:
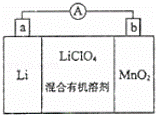
锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原 理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
(1)外电路的电流方向是由b极流向 极(填字母).
(2)电池正极反应式 .
(3)是否可用水代替电池中的混合有机溶剂?否(填“是”或“否”),原因是 .
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为 .K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 .
查看答案和解析>>
科目: 来源: 题型:
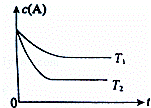
反应A(g)⇌B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如右图所示.回答下列问题:
(1)上述反应的温度T1小于 T2,平衡常数K(T1) K(T2).(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为 .
②反应的平衡常数K= .
③反应在0~5min区间的平均反应速率v(A)= .
查看答案和解析>>
科目: 来源: 题型:
认真观察下列装置,回答下列问题:
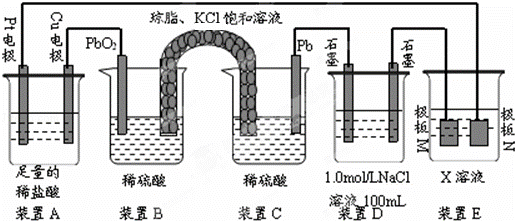
(1)装置B中PbO2上发生的电极反应方程式为 .
(2)装置A中总反应的离子方程式为 .
(3)若装置E中的目的是在Cu材料上镀银,则X为 ,极板N的材料为Ag.若装置E的目的是验证金属的电化学防腐,则极板N的材料为 .
(4)当装置A中Cu电极质量改变6.4g时,装置D中产生的气体体积为 L(标准状况下).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com