
科目: 来源: 题型:
下列叙述中正确的是( )
|
| A. | 在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
|
| B. | 元素由化合态变为游离态的反应一定是还原反应 |
|
| C. | 置换反应一定是氧化还原反应 |
|
| D. | 失电子难的原子,一定容易得电子,反之成立 |
查看答案和解析>>
科目: 来源: 题型:
下列电离方程式错误的是( )
|
| A. | K2CO3=2K++CO32﹣ | B. | KClO3=K++ClO3﹣ |
|
| C. | H2CO3⇌2H++CO32﹣ | D. | NaHCO3=Na++HCO3﹣ |
|
| E. | K2CO3=2K++CO32﹣ |
|
|
查看答案和解析>>
科目: 来源: 题型:
为了测定某铜银合金的成分,将30.0g合金溶于80ml13.5mol/L的浓硝酸中,待合金完全溶解后,收集到标况气体6.72L,并测得溶液的C(H+)=1moL/L,假设反应后溶液的体积仍为80mL,计算:
(1)被还原的硝酸的物质的量.
(2)合金中银的质量分数.
查看答案和解析>>
科目: 来源: 题型:
某学生设计的用氨催化法制取少量HNO3溶液的实验装置如图所示: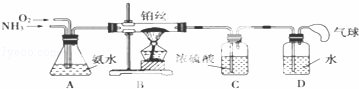
(1)实验室制备NH3,下列方法中适宜选用的是 (填序号).
①固态氯化铵与熟石灰混合加热
②固态氯化铵加热分解
③碱石灰中滴加浓氨水
④氯化铵溶液与氢氧化钠溶液共热
(2)装置B中发生反应的化学方程式为 .在实验过程中,加热铂丝红热后,移去酒精灯,发现铂丝还继续保持红热,由此可判断该反应是 (填“吸热”或“放热”)反应.
(3)装置C的作用是 ;装置C中的现象是 ;为确保装置D中尽可能多地生成HNO3,所通入O2和NH3的体积比应大于 .
(4)装置D中发生的反应方程式为 .
查看答案和解析>>
科目: 来源: 题型:
如图:a、b、c、d均为铂电极,供选择的四组电解液如下:
组 A B C D
甲槽 NaOH AgNO3 H2SO4 NaCl
乙槽 CuSO4 CuCl2 AgNO3 AgNO3
要求满足的条件是:
(a)工作一段时间后,甲槽电解液pH值上升,乙槽电解液的pH值下降
(b)a、d两极放电离子的物质的量相等
请填写下列空格:
(1)应选用的电解液是哪一组D;(填字母)
(2)甲槽的电解方程式 .
(3)当a极析出3.55g电解产物时,d极上将析出 g物质.

查看答案和解析>>
科目: 来源: 题型:
2(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 .
(2)肼﹣空气燃料电池是一种碱性燃料电池,电解质溶液是KOH溶液.肼﹣空气燃料电
池放电时:正极的电极反应式是 ;负极的电极反应式是 .
(3)如图是一个电化学过程示意图.假设使用肼﹣空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
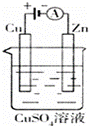
查看答案和解析>>
科目: 来源: 题型:
已知下列几种化学键的键能:
化学键 Si﹣Si键 H﹣H键 Cl﹣Cl键 H﹣Cl键 Si﹣Cl键
键能(KJ/mol) 176 436 243 431 360
请计算下列反应的反应热:
(1)H2(g)+Cl2(g)=2HCl(g)△H= ;
(2)50mL 0.50mol•L﹣1盐酸与50mL 0.55mol/L NaOH溶液简易量热计中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(a)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”).
(b)酸、碱混合时,把量筒中的NaOH溶液缓缓倒入小烧杯中测得的中和热的数值会 .(填“偏大”“偏小”“无影响”)
(c) 实验中用环形铜丝搅拌棒代替 ,测得的中和热的数值会 .(均填“偏大”“偏小”“无影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com