
科目: 来源: 题型:
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的离子方程式有 ;
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应中,收集产生的气体,记录获得相同体积的气体所需时间.
实验 A B C D E F
混
合
溶
液 4mol/LH2SO4/mL 30 V1 V2 V3 V4 V5
饱和CuSO4/mL 0 0.5 2.5 5 V6 20
H2O/mL V7 V8 V9 V10 10 0
时间(min) 15 10 5 3 6 9
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因 ;
(3)改用锌粉与稀硫酸反应,加入少量硫酸铜溶液后充分振荡,一段时间剩余少量固体.该同学对固体成分提出下列假设:
假设1:全部为铜;
假设2: .
(4)请你设计实验验证上述假设1,完成下表内容.
实验方案(不要求写具体操作过程) 预期实验结果和结论
,
查看答案和解析>>
科目: 来源: 题型:
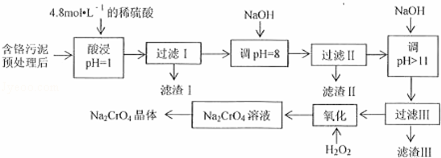
某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺流程如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Mg2+):
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO42﹣形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀是溶液的pH如下:
阳 Fe Mg Al Cr
开始沉淀时的H 1.9 9.0 ﹣﹣ ﹣﹣
沉淀完全时的H 3. 11.1 8 9(>9溶解)
(1)实验室用18.4mol•L﹣1的浓硫酸配制250mL 4.8mol•L﹣1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需量 ;
(2)滤渣II是 ,过滤II步骤能否省略,为什么?
.
(3)写出滤液中加入H2O2发生反应的两种方程式 ;
(4)取得到的Na2CrO4晶体0.48g,加入硫酸溶液得到Na2CrO溶液,用0.3000 mol•L﹣1滴定至终点时(铬被还原为Cr3+),消耗20.00mL标准溶液.
①盛装FeSO4标准溶液应用酸式滴定管(填“酸式”或“碱式”),滴定时的操作为:
②计算该产品中Na2CrO4的质量分数为 .
查看答案和解析>>
科目: 来源: 题型:
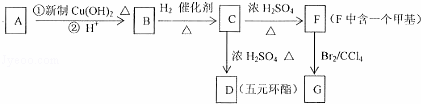
某有机物A的分子式为C5H8O2,A中碳链无支链,1mol A能与2mol H2发生加成反应,但不能与溴水发生加成反应,根据下面转化关系回答下列问题:
(1)C的分子式为 ;
(2)A的结构简式为 ,D的核磁共振氢谱图中将出现 种峰;
(3)G中所含官能团的名称为 ;
(4)B→C的反应类型是 ,C→D的反应类型 ;(选择填空)
a.消去反应 b.加成反应 c.还原反应 d.酯化反应
(5)写出G与NaOH溶液反应的化学方程式: ;
(6)M是F的同系物,其相对分子质量比F小14,写出满足条件的M的所有可能的结构(不包括顺反异构) .
查看答案和解析>>
科目: 来源: 题型:
C、O、Si、Cl、Na、Fe是中学化学中常见的六种元素.
(1)Si位于元素周期表第三周期第ⅣA族,Fe2+的离子结构示意图 ,Cl的基态原子外围电子层排布式为 ;
(2)用“>”或“<”填空:
第一电离能 键能 沸点
O Na H﹣Cl H﹣Si CO2 H2O
(3)氯的一种常见含氧酸有漂白性,它与H2CO3酸性强弱不同,写出可以证明此结论一个化学方程式 ;
(4)黄绿色气体二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.工业上常利用氯酸钠和浓盐酸来制备ClO2,同时还得到一种黄绿色的气体单质、一种无色液体和一种常见离子化合物.写出该反应的化学方程式,并标出电子转移的方向和数目: ;
(5)Ti倍称为继铁铝之后“21世纪”金属,应用前景很广.钛铁矿(FeTiO3)可被一氯化碳还原为铁和TiO2固体.在25℃、101KPa下,已知煤消耗7克CO,吸收aKJ热量,该反应的热化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是()
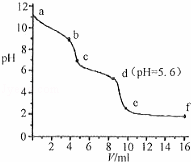
A. a点时,溶液呈碱性的原因是CO32﹣发生水解反应,其离子方程式为:CO32﹣+2H2O=H2CO3+2OH﹣
B. a→b段,溶液有气体放出
C. c点以后,盐酸过量
D. d点溶液中c(Na+)=c(Cl﹣)
查看答案和解析>>
科目: 来源: 题型:
室温下,下列溶液中粒子浓度大小关系正确的是()
A. Na2S溶液中,2c(Na+)=c(S2﹣)+c(HS﹣)+c(H2S)
B. 强碱弱酸盐NaA溶液的pH=8,则c(OH﹣)﹣c(HA)=1,0×10﹣8mol/L
C. KAl(SO4)2溶液中,c(SO42﹣)>c(K+)=c(Al3+)>c(H+)>c(OH﹣)
D. 向100ml pH=12 的 NaOH溶液中加入pH=2的醋酸溶液至中性,所得溶液的总体积大于200ml
查看答案和解析>>
科目: 来源: 题型:
某聚合物锂离子充电电池放电时的反应为:Li1﹣xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是()
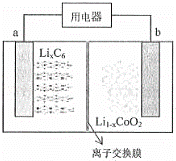
A. 放电时,电子从b极流向a极
B. 放电时,a极脱出的离子通过阴离子交换膜从左向右移动
C. 充电时,b极发生的反应为:LiCoO2﹣xe﹣=Li1﹣xCoO2+xLi+
D. 充电时,每转移x mol 电子,产生6mol碳单质
查看答案和解析>>
科目: 来源: 题型:
一定条件下,在容积固定不变的密闭容器中加入一定量的X和Y进行如下可逆反应,2X(g)+Y(s)⇌Z(g)+W(g)△H>0,一段时间后达到化学平衡状态后,再改变某一条件,下列有关叙述正确的是()
A. 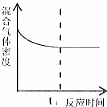
t1时刻表示该可逆反应达到新的平衡
B. 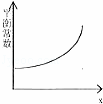
横坐标x可表示温度或容器的体积
C. 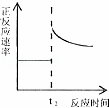
t2时刻改变的体积为加入少量的Y
D. 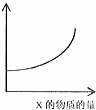
横坐标可表示为Z的体积分数
查看答案和解析>>
科目: 来源: 题型:
为实现下列实验目的,下表所提供的实验仪器和试剂都会用到且都正确的是()
选项 实验目的 主要仪器 试剂
A 测定中和热 量筒、温度计、酒精灯 盐酸、NaOH溶液
B 制备氢氧化铁胶体 烧杯、胶头滴管 饱和FeCl3溶液
C 配制10%CuSO4溶液100g 100ml 容量瓶、玻璃棒 胆矾
D 实验室制取、收集干燥的氮气 大试管、酒精灯 氯化铵、消石灰、无水CaCl2
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
复盐NH4Fe(SO4)2俗称铁铵矾,下列有关其溶液的叙述正确的是()
A. 该溶液中K+、Mg2+、H+、NO3﹣不能大量共存
B. 溶液中的NH4+与Fe3+均发生水解反应,且相互促进
C. 加入金属铜与Fe3+反应的离子方程式为:2Fe3++3Cu=2Fe+3Cu2+
D. 向其中滴入Ba(OH)2溶液恰好使SO42﹣完全沉淀:NH4++Fe3++2SO42﹣+2Ba2++4OH﹣=2BaSO4↓+NH3•H2O+Fe(OH)3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com