
科目: 来源: 题型:
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是()
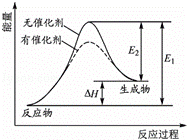
A. 该反应为吸热反应
B. 催化剂能改变反应的焓变
C. 催化剂能降低反应的活化能
D. 逆反应的活化能大于正反应的活化能
查看答案和解析>>
科目: 来源: 题型:
关于热化学方程式:2H2(g)+02(g)=2H20(1),△H=﹣571.6kJ•mol﹣1,下列有关叙述不正确的是()
A. 2mol H2完全燃烧生成液态水时放出571.6 kJ的热
B. 1mol H2完全燃烧生成液态水时放出285.8kJ的热
C. 2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D. 上述热化学方程式可表示为H2(g)+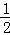 O2(g)=H20(1),△H=﹣285.8 kJ•mol﹣1
O2(g)=H20(1),△H=﹣285.8 kJ•mol﹣1
查看答案和解析>>
科目: 来源: 题型:
下列有关化学反应速率的说法中,正确的是()
A. 100mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B. 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
C. 二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢
D. 汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢
查看答案和解析>>
科目: 来源: 题型:
下列反应符合如图p﹣υ变化曲线的是()

A. H2(g)+I2(g)⇌2HI(g) B. 3NO2(g)+H2O(l)⇌2HNO3(l)+NO(g)
C. 4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) D. CO2(g)+C(s)⇌2CO(g)
查看答案和解析>>
科目: 来源: 题型:
对于反应中的能量变化,表述正确的是()
A. 放热反应中,反应物的总能量大于生成物的总能量
B. 断开化学键的过程会放出能量
C. 加热才能发生的反应一定是吸热反应
D. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
查看答案和解析>>
科目: 来源: 题型:
在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)⇌2HI(g)△H<0反应中各物质的浓度随时间变化情况如图1:
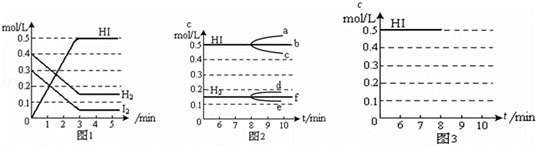
(1)该反应的化学平衡常数表达式为K= .
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K (填写“增大”、“减小”或“不变”)HI浓度的变化正确的是 (用图2中a﹣c的编号回答)
②若加入I2,H2浓度的变化正确的是 ,(用图2中d﹣f的编号回答)
(3)反应达到平衡后,第8分钟时,若反应容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况.
查看答案和解析>>
科目: 来源: 题型:
已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/℃ 700 900 830 1000 1200
平衡常数 1.7 1.1 1.0 0.6 0.4
回答下列问题:
(1)该反应的△H 0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,若反应经一段时间后,达到平衡时A的转化率为80%,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率会 (填“变大”、“变小”或“不变”)
(3)若保持容器的容积不变,则该反应达到化学平衡状态的依据是 (填序号).
a.单位时间里生成B和D的物质的量相等
b.气体的密度不随时间改变
c.容器内压强保持不变
d.混合气体的平均摩尔质量保持不变
(4)1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的 值为 .
值为 .
查看答案和解析>>
科目: 来源: 题型:
据报道,摩托罗拉公司开始了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.如图是一个电化学过程的示意图.已知甲池总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O
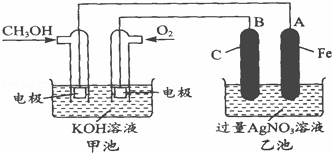
请填空:
(1)充电时:①原电池的负极与电源负极相连.②阳极的电极反应式为
(2)放电时,负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质增加648g,则甲池中理论上消耗O2 L(标准状况下).
查看答案和解析>>
科目: 来源: 题型:
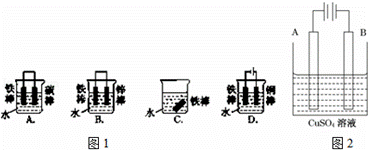
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一.请回答钢铁在腐蚀、防护过程中的有关问题.
(1)图1哪个装置可防止铁棒被腐蚀BD.
(2)在实际生产中,可在铁 件的表面镀铜防止铁被腐蚀.装置示意图如图2. 请回答
件的表面镀铜防止铁被腐蚀.装置示意图如图2. 请回答
①A电极对应的金属是铜(写元素名称),B电极的电极反应式是 .
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因 .
查看答案和解析>>
科目: 来源: 题型:
依据事实,写出下列反应的热化学方程式.
(1)已知拆开1mol H﹣H键,1mol N﹣H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为: .
(2)以甲烷为原料制取氢气是工业上常用的制氢方法.
已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ•mol﹣1
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com