
科目: 来源: 题型:
有一瓶澄清的溶液,可能含NH4+、K+、Na +、Mg2+、Ba2+、Al3+、Fe3+、SO42﹣、CO32﹣、Cl﹣、I﹣中的一种或几种,取该溶液进行如下实验:
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,CCl4层呈紫红色;
(3)取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
(4)取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实确定并回答:在溶液中肯定存在的离子有 ,肯定不存在的离子有 ,还不能确定是否存在的离子有 .
查看答案和解析>>
科目: 来源: 题型:
工业上用黄铜矿( CuFeS2)冶炼铜,副产品中也有SO2,冶炼铜的反应为:8CuFeSO2+2IO2 8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中 Fe 的化合价为+2,反应中被还原的元素是 (填元素符号).当生成0.8mol铜时,此反应转移的电子数目是 .
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中 Fe 的化合价为+2,反应中被还原的元素是 (填元素符号).当生成0.8mol铜时,此反应转移的电子数目是 .
查看答案和解析>>
科目: 来源: 题型:
在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是 . 在上述蓝色溶液中,继续滴加足量的NaClO溶液,蓝色逐渐消失,有关反应的离子方程式是 .(提示:碘元素被氧化成IO3﹣)从以上实验可知,ClO﹣、I2、IO3﹣的氧化性由强到弱的顺序是 .
查看答案和解析>>
科目: 来源: 题型:
煤炭中以FeS2形式存在的硫,在有水和空气及在脱硫微生物存在下发生生物氧化还原反应,有关反应的离子方程式依次为:
①2FeS2+7O2+2H2O 4H++2Fe2++4SO42﹣;
4H++2Fe2++4SO42﹣;
②4Fe2++O2+4H+ 4Fe3++2H2O;
4Fe3++2H2O;
③FeS2+2Fe3+ 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O 4H++2
4H++2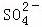 .
.
已知:FeS2中的铁元素为+2价.
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述①②离子方程式补充完整.
(2)反应③的还原剂是 .
(3)观察上述反应,FeS2最终转化为 从煤炭中分离出来.
查看答案和解析>>
科目: 来源: 题型:
下列实验基本操作或说法正确的是 (填写序号)
A、用50ml的量筒量取5.2ml稀硫酸
B、为了有效地除去粗盐中的Ca2+、Mg2+、SO42﹣,可先加入NaOH,再加入BaCl2,最后加入Na2CO3,将沉淀过滤后,再用HCl调整溶液至中性
C、石蕊试纸或PH试纸使用前都应用蒸馏水润湿
D、稀释浓硫酸时,应将水沿器壁缓缓加入浓硫酸中,并不断用玻璃棒搅拌
E、容量瓶中含有少量蒸馏水,对配制一定物质的量浓度的硫酸溶液无影响
F、将饱和FeC13溶液滴加沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体;
G、乙酸乙酯制备收集完毕,分液时,直接将乙酸乙酯从分液漏斗的上口倒出
H、在粗盐的提纯实验中,溶解、过滤、蒸发都用到了玻璃棒.
查看答案和解析>>
科目: 来源: 题型:
为确定某溶液的离子组成,分别进行如下实验:
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验以下推测正确的是()
A. 一定有SO32﹣离子
B. 一定有CO32﹣离子
C. 一定有Cl﹣离子存在
D. 不能确定HCO3﹣离子是否存在
查看答案和解析>>
科目: 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂.工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3+3ClO﹣+4OH﹣=2FeO42﹣+3Cl﹣+5H2O,
干法制备的主要反应方程为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
则下列有关说法正确的是()
A. 高铁酸钾中铁显+6价
B. 湿法中FeO42﹣是还原产物
C. 干法中每生成1mol Na2FeO4 转移4mol电子
D. K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质
查看答案和解析>>
科目: 来源: 题型:
下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2•6H2O晶体后,仍能大量共存的是()
A. Na+、H+、Cl﹣、NO3﹣ B. Na+、Mg2+、Cl﹣、SO42﹣
C. K+、Ba2+、OH﹣、I﹣ D. Cu2+、CO32﹣、Br﹣、ClO﹣
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式与所述事实相符且正确的是()
A. 漂白粉溶液在空气中失效:ClO﹣+CO2+H2O═HClO+HCO3﹣
B. 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl﹣ Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C. 用小苏打治疗胃酸过多:HCO3﹣+H+=CO2↑+H2O
D. 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO﹣+2Fe(OH)3═2FeO42﹣+3Cl﹣+H2O+4H+
查看答案和解析>>
科目: 来源: 题型:
下列反应最终能生成Fe3+的化合物的是()
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
A. ①②③ B. ①③⑤ C. ③④ D. ③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com