
科目: 来源: 题型:
根据热化学方程(在101kpa时):S(s)+O2(g)=SO2(g);H=﹣297.23kJ/mol,分析下列说法中不正确的是()
A. S的燃烧热为297.23KJ/mol
B. S(s)+O2(g)=SO2(g)放出的热量大于297.23kJ
C. S(s)+O2(g)=SO2(g)放出的热量小于297.23kJ
D. 形成1mol二氧化硫的化学键所释放的总能量大于断裂1molS和1molO2的化学键所吸收的总能量
查看答案和解析>>
科目: 来源: 题型:
下列叙述中正确的是()
A. 在稀溶液中,1mol酸和1mol碱完全反应所放出的热量,叫做中和热
B. 热化学方程式中,各物质前的化学计量数不表示分子个数
C. 在101kPa时,1mol物质燃烧时所放出的热量叫做该物质的燃烧热
D. 如果反应物所具有的总能量小于生成物所具有的总能量,则反应放热
查看答案和解析>>
科目: 来源: 题型:
某元素的同位素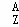 X,其氯化物XCl2 1.11g配成溶液后,需用1mol/L的AgNO3溶液20mL才能把氯离子完全沉淀下来.已知同位素中有20个中子.
X,其氯化物XCl2 1.11g配成溶液后,需用1mol/L的AgNO3溶液20mL才能把氯离子完全沉淀下来.已知同位素中有20个中子.
(1)计算X的质量数为多少?
(2)指出X元素在周期表中的位置.
查看答案和解析>>
科目: 来源: 题型:
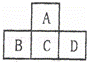
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素的原子核外共有56个电子,在周期表中的位置如图所示.E元素的最高价氧化物既能与强酸反应又能与强碱反应.请回答:
(1)写出下列元素的元素符号:A 、B 、D .
(2)A元素与氢元素形成的H2A化合物分子中,所含化学键为 键(填“离子”或“极性”或“非极性”),用电子式表示H2A的形成过程 , .
(3)A元素与E元素形成的化合物的化学式是 ,该化合物在物质分类中属于 氧化物.(填“酸性”,“碱性”或“两性”)
(4)向D元素与E元素形成的化合物的水溶液中滴加NaOH溶液,开始时,实验现象是 有 ,反应的离子方程式为 ;继续滴加NaOH溶液至过量,实验现象是 .
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C均为短周期元素,A、B两种元素的原子具有相同数目的电子层,A元素原子最外层电子数是B元素原子最外层电子数的两倍,A元素原子M层电子数为K层电子数的3倍,C元素原子的核电荷数是电子层数的4倍,其质子数为最外层电子数的6倍.请完成下列空白:
(1)A元素为 ,C元素为 ,B元素的名称为 .
(2)A位于元素周期表中第 周期第 族
(3)C的离子结构示意图为
(4)A、B、C三种元素形成的原子半径由大到小的顺序是 (化学符号)
(5)A、B、C三种元素最高价氧化物对应的水化物中分别为 、 、 .
查看答案和解析>>
科目: 来源: 题型:
分别由氕(1H)、氘(2H)、氚(3H)组成的单质(均为双原子分子),其质量均为1g,则它们:
(1)原子个数比为 .
(2)电子个数比为 .
(3)相同条件下的密度之比为 .
(4)相同条件下的体积之比为 .
查看答案和解析>>
科目: 来源: 题型:
元素周期表中,同主族元素从上到下,原子半径逐渐 (填“增大”或“减小”),元素的金属性逐渐 (填“增强”或“减弱”),非金属性逐渐 (填“增强”或“减弱”);同周期从左到右,原子半径逐渐 (填“增大”或“减小”),元素的金属性逐渐 (填“增强”或“减弱”),非金属性逐渐 (填“增强”或“减弱”).
查看答案和解析>>
科目: 来源: 题型:
已知短周期元素形成的离子aA+、bB2+、cC﹣、dD2﹣均具有相同的电子层结构,下列判断正确的是( )
|
| A. | 元素的金属性:B>A;元素的非金属性:D>C |
|
| B. | 原子序数:b>a>c>d |
|
| C. | 离子半径:D2﹣>C﹣>B2+>A+ |
|
| D. | 原子半径:A>B>C>D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com