
科目: 来源: 题型:
有关短周期元素A、B、C、D、E、F的信息如下:
元素 有关信息
A 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐
B 最外层电子数是次外层电子数的2倍
C M层上有3个电子
D 短周期原子半径最大的主族元素
E 其单质是淡黄色固体
F 最高正价与最低负价代数和为6
请回答下列问题:
(1)写出基态A原子外围电子的电子排布图 .气态氢化物乙中A原子的杂化类型是SP3.
(2)E、F两元素的电负性大小比较:E F(选填>、<或=)
(3)下列说法正确的是 (填序号).
①实验室可用右图所示装置制取B的最高价氧化物.
②用C单质做成的槽车,都可用来运输甲的浓溶液.
③C形成的单质熔点低于D形成的单质的熔点.
④E的氢化物稳定性强于F的氢化物稳定性.
(4)将E的常见氧化物(该氧化物能使品红溶液褪色)通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,可知其中含Cl:35.7%,Cu:64.3%,则该氧化物在上述反应中的作用是 .
A.漂白剂B.氧化剂C.还原剂.

查看答案和解析>>
科目: 来源: 题型:
下面的表格是元素周期表的一部分,其中的序号对应的是元素.
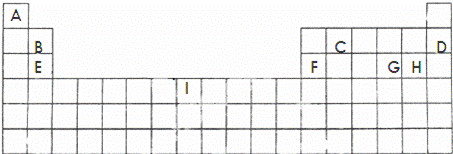
请回答下列问题:
(1)按原子轨道的重叠方式看,元素A、C形成的相对分子质量最小的分子含 键;元素E和H形成的化学键类型为 .
(2)上表中所列举的某元素最外电子层上p电子数比s电子数少1,则该元素的元素符号为
(3)B、D、E、F四种元素的第一电离能由大到小的顺序是(填元素符号) .
(4)元素I的价电子排布式为 .I元素通常情况下能形成两种离子,其中较稳定的是Fe3+,其原因是 .
(5)硒(se)是人体必需的微量元素,与G同一主族,Se原子比G原子多一个电子层.则:Se的原子序数为34,其原子结构示意图为 .
(6)G、H两元素能形成G2H2,它是一种琥珀色液体,是合成硫化染料的重要原料.它的熔点﹣80℃,沸点138℃.常温下,它遇水易反应,产生使品红褪色的气体,且溶液出现浑浊.
①S2Cl2遇水反应产生气体,该气体分子是 (填“极性”或“非极性”)分子.
②写出二氯化硫与水反应的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
A、X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;A原子价电子排布式nsnnpn+1,X2﹣和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.回答下列问题(相关回答均用元素符号表示):
(1)R基态原子的核外电子排布式是 .W在周期表中的位置是
(2)NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是 (填字母).
A.离子键B.极性键C.配位键 D.金属键
(3)A原子的第一电离能 (填“大于”、“小于”或“等于”)X原子的第一电离能; A元素的氢化物是一种易液化的气体,该气体易液化的原因是
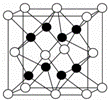
(4)X与Y形成的化合物Y2X2的电子式 ,其晶体类型是 .X与Y形成的化合物的晶胞如图所示,则该化合物的化学式为 (请用推断出的元素符号表示).
(5)Z的某种含氧酸盐常用于实验室制取X形成的单质,此酸根离子的空间构型为 .
查看答案和解析>>
科目: 来源: 题型:
含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O.
(1)与OH﹣互为等电子体的一种分子为HF(填化学式).
(2)葡萄糖等很多不饱和有机物在Ni催化下可以与H2发生加成反应.如①CH2=CH2 ②CH≡CH③ ④HCHO等,
④HCHO等,
其中Ⅰ:①中含有的官能团名称是 、③的分子式为 .
Ⅱ:②中碳原子的轨道杂化类型是 ;④的立体构型为 .
(3)Cu属于 区元素,基态Cu+核外价电子排布式为
铜的另一种价态的离子Cu2+的水合离子中,提供孤电子对的原子是 .
(4)将氨气通入到Cu(OH)2悬浊液的离子方程式为 .
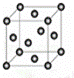
(5)Cu2O在稀硫酸中生成Cu和CuSO4,请写出该反应的化学方程式: .铜晶胞结构如右图所示,铜晶体中每个铜原子周围等距离且最近的铜原子数目为 .
查看答案和解析>>
科目: 来源: 题型:
根据已学知识,请你回答下列问题:
(1)试比较含氧酸的酸性强弱(填“>”、“<”或“=”):HClO3 HClO4.
(2)根据价层电子对互斥理论判断:H2O的VSEPR构型为正四面体H3O+的分子立体结构为三角锥.
(3)沸点比较:邻羟基苯甲醛 对羟基苯甲醛(填“>”、“<”或“=”)
(4)在下列物质①NH3、②BF3、③HCl、④SO3,属于非极性分子的是(填番号) .
(5)①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有(填序号).
(6)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体为 .
(7)配离子[TiCl(H2O)5]2+的中心离子的符号为 ,配位数为 .
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9,单质Y可与NaOH溶液反应生成氢气.下列说法不正确的是()
A. 原子半径:Y>Z>W
B. XW2熔点为107℃,沸点为142.5℃,说明固态XW2为分子晶体
C. 电解YW3固体可得单质Y
D. 
ZW2分子结构见右图,说明ZW2是极性分子
查看答案和解析>>
科目: 来源: 题型:
SCR法(选择性催化还原技术)是一种以NH3作为还原剂,将烟气中NOx分解成无害的N2和H2O的干法脱硝技术,反应原理为:①6NO+4NH3═5N2+6H2O;②6NO2+8NH3═7N2+12H2O;③NO+NO2+2NH3═2N2+3H2O.下列说法正确的是()
A. 汽车尾气中含有NOx,NOx是引起温室效应的主要气体之一
B. N2中π键与σ键之比为1:2
C. 反应③中每生成标况下的22.4 L N2转移电子数1.5NA
D. NH3的沸点比PH3的沸点高
查看答案和解析>>
科目: 来源: 题型:
下列说法全部正确的是()
①CH3﹣CH=CH2和CH2=CH2的最简式相同;
②CH≡CH和C6H6含碳量相同;
③苯乙烯和丁烯为同系物;
④正戊烷、异戊烷、新戊烷的沸点逐渐变低;
⑤标准状况下,11.2L的戊烷所含的分子数为0.5NA (NA为阿伏加德罗常数)
A. ①②③ B. ②③④ C. ①②④ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是()
①具有规则几何外形的固体一定是晶体
②含有阳离子的晶体一定是离子晶体
③非极性分子中一定含有非极性键
④s﹣s σ键与s﹣p σ键的电子云形状相同
⑤含有共价键的晶体一定具有高的熔、沸点及硬度
⑥因为H﹣F的键能大于H﹣Cl的键能,所以HF的沸点高于HCl
⑦含有π键的化合物与只含σ键的化合物的化学性质不同
⑧中心原子采取sp3杂化的分子,其立体构形不一定是正四面体.
A. ①②⑤⑥ B. ③⑦⑧ C. ⑦⑧ D. ③④⑤⑧
查看答案和解析>>
科目: 来源: 题型:
下面的排序不正确的是()
A. 晶体熔点由低到高:CH4<SiH4<GeH4<SnH4
B. 熔点由高到低:Rb>K>Na
C. 硬度由大到小:金刚石>碳化硅>晶体硅
D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com