
科目: 来源: 题型:
氯气是一种重要的工业原料.工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
|
| A. | 若管道漏气遇氨就会产生白烟 |
|
| B. | 该反应利用了Cl2的强氧化性 |
|
| C. | 该反应属于复分解反应 |
|
| D. | 生成1mol N2有6mol电子转移 |
查看答案和解析>>
科目: 来源: 题型:
一元硬币的外观有银白色的金属光泽,一些同学认为它可能是铁制成的,为证明其想法,有同学拿磁铁来吸引一下.就这一过程而言,属于科学探究中的( )
|
| A. | 实验 | B. | 假设 | C. | 观察 | D. | 做结论 |
查看答案和解析>>
科目: 来源: 题型:
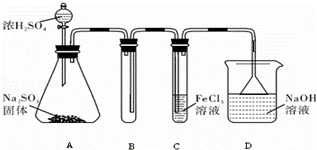
某研究小组用下图装置进行SO2 与FeCl3溶液反应的相关实验(夹持装置已略去).
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释,这样操作的目的是 ,操作中不需要的仪器有 (填字母).
a.药匙 b.烧杯 c.石棉网 d.玻璃棒 e.坩埚
(2)通入足量SO2时C中观察到的现象为 ,
(3)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应.
①写出SO2与FeCl3溶液反应的离子方程式 ;
②请设计实验方案检验有Fe2+生成取 ;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42﹣.该做法 (填“合理”或“不合理”),理由是 .
(4)D装置中倒置漏斗的作用是 .
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有 (填入正确选项前的字母).
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液.
查看答案和解析>>
科目: 来源: 题型:
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既价廉又环保.

(1)工业上可用组成为K2O•M2O3•2RO2•nH2O的无机材料纯化制取的氢气
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为
②常温下,不能与M单质发生反应的是 (填序号)
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气来的方法有多种
①高温热分解法
已知:H2S(g)⇌H2(g)+1/2S2(g)
在恒温密闭容器中,控制不同温度进行H2S分解实验.以H2S起始浓度均为cmol•L﹣1测定H2S的转化率,结果见右图.图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率.据图计算985℃时H2S按上述反应分解的平衡常数K= ;说明随温度的升高,曲线b向曲线a逼近的原因:
;说明随温度的升高,曲线b向曲线a逼近的原因:
②电化学法
该法制氢过程的示意图如右.反应池中反应物的流向采用气、液逆流方式,其目的是 ;反应池中发生反应的化学方程式为 .反应后的溶液进入电解池,电解总反应的离子方程式为 .
查看答案和解析>>
科目: 来源: 题型:
面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景.
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)⇌CH3OH(g)△H1=﹣90kJ•mol﹣1
②CO(g)+H2O(g)⇌CO2(g)+H2(g)△H2=﹣41kJ•mol﹣1
写出由二氧化碳、氢气制备甲醇的热化学方程式: .
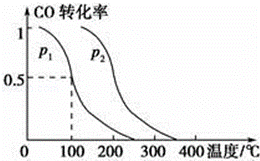
(2)在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示.
①p1 小于p2(填“大于”、“小于”或“等于”);
②在其他条件不变的情况下,再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率(填“增大”、“减小”或“不变”,下同),平衡常数 .
(3)已知在T℃时,CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1mol•L﹣1,c始(H2O)=1mol•L﹣1,某时刻经测定CO的转化率为10%,则该反应没有(填“已经”或“没有”)达到平衡,原因是Qc K,此时刻v正 v逆(填“>”或“<”).
查看答案和解析>>
科目: 来源: 题型:
全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42﹣.电池放电时,负极的电极反应为:V2+﹣e﹣=V3+.
①电池放电时的总反应方程式为 .充电时,电极M应接电源的 极.
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+.则第一步反应过程中阴极区溶液n(H+) (填“增大”、“不变”或“减小”),
阳极的电极反应式为 .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com