
科目: 来源:模拟题 题型:单选题
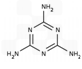 ,俗称“蛋白精”)一样都是蛋白 质,但明胶可用于食品工业的添加剂,而三聚氰胺不可用于食品加工
,俗称“蛋白精”)一样都是蛋白 质,但明胶可用于食品工业的添加剂,而三聚氰胺不可用于食品加工  2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增大
2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增大 查看答案和解析>>
科目: 来源:模拟题 题型:填空题
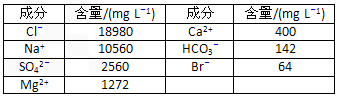
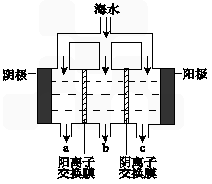
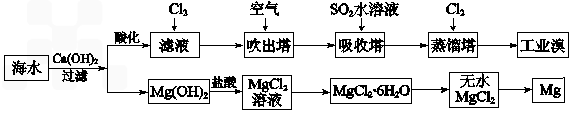
查看答案和解析>>
科目: 来源:福建省期中题 题型:填空题

查看答案和解析>>
科目: 来源:湖北省期中题 题型:单选题


查看答案和解析>>
科目: 来源:山东省期中题 题型:单选题
查看答案和解析>>
科目: 来源:同步题 题型:不定项选择题
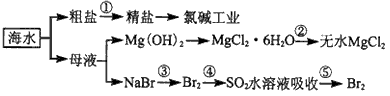
[ ]
查看答案和解析>>
科目: 来源:河北省模拟题 题型:填空题
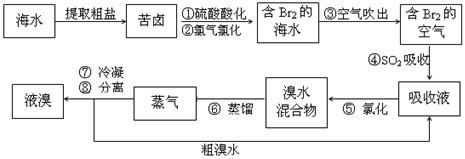
查看答案和解析>>
科目: 来源:期末题 题型:单选题
查看答案和解析>>
科目: 来源:同步题 题型:填空题

查看答案和解析>>
科目: 来源:同步题 题型:实验题
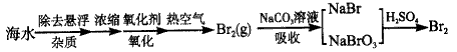
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com