
科目: 来源: 题型:
I.X是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
(1)若X为氧化物,则X的化学式为_____________。
(2)若X为单质,写出其与NaOH溶液反应的化学方程式_____________。
(3)若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。
常温下X与足量稀氢氧化钠溶液反应的离子方程式为_____________。
II. 在一定条件下进行的下列化学反应,请根据以下的转化关系回答下列问题。已知A、B、C中均含有同种元素。
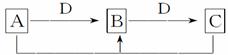
(1)若D为金属单质,且以上反应均为氧化还原反应,转化过程中没有除A、B、C外的其他物质生成,请写出A+C→B反应的离子方程式__________。
(2)在常温下,若B、D为非金属单质,A是有臭鸡蛋气味的气体,请写出A+C→B反应的化学方程式__________。
(3)若D为碱,且以上反应均为非氧化还原反应,则A、B、C、D分别可以是:(按顺序写出合理的一组物质的化学式即可)A________,B________,C________,D________。
查看答案和解析>>
科目: 来源: 题型:
将x mol Al2O3和y mol CuO混合后,全部溶于V L过量的稀硫酸中,然后向溶液中逐渐加入0.5 mol/L的NaOH溶液,当加入a L时,生成的沉淀最多,则原稀H2SO4的物质的量浓度为( )
| |
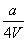 mol/L B.
mol/L B.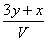 mol/L C.
mol/L C.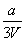 mol/L D.
mol/L D.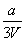 mol/L
mol/L 查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是( )
A.原子半径:W>Z>Y>X>M
B.XZ2、X2M2、W2Z2均为直线型的共价化合物
C.由X元素形成的单质不一定是原子晶体
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目: 来源: 题型:
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
 A.若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶
A.若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶
液变浑浊
B.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
C.若A为浓氨水,B为生石灰,C中盛A1C13溶液,则C中
先产生白色沉淀后沉淀又溶解
D.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色
查看答案和解析>>
科目: 来源: 题型:
在t℃时,将a gNH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρg/mL,质量分数为ω,其中含NH4+的物质的量为bmol。下列叙述中正确的是( )
A.溶质的质量分数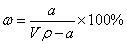
B.溶质的物质的量浓度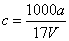 mol/L
mol/L
C.溶液中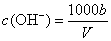 mol/L
mol/L
D.题述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是( )
A.往石灰乳中通入过量的CO2:OH-+CO2=HCO3-
B.a mol FeBr2溶液中通入a mol Cl2:
2Fe2++2Br-+2Cl2 = Br2+2Fe3++4C1-
C.碳酸氢钙溶液加到醋酸中:
Ca(HCO3)2+2CH3COOH=Ca2++2CH3COO-+2CO2↑+2H2O
D.向50 mL 1 mol·L-1明矾溶液中滴入数滴0.1 mol·L-1Ba(OH)2溶液
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
科目: 来源: 题型:
体积为1L的干燥容器中充入一定量HCl气体后,测得容器中气体对氧气的相对密度为1.082。则容器中HCl气体的质量分数约为( )
A.75% B.25% C.79.1% D.78.1%
查看答案和解析>>
科目: 来源: 题型:
已知溶质质量分数为98%的浓硫酸,其物质的量浓度为18.4mol/L,取10mL该硫酸与a mL水混合,配制成溶质质量分数为49%的硫酸,其物质的量浓度为bmol/L,则a,b分别为( )
A.a = 10 b = 9.2 B.a < 10 b > 9.2
C.a > 10 b = 9.2 D.a > 10 b < 9.2
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是 ( )
①将CO2通入溶有足量氨的BaCl2溶液中,无白色沉淀生成
②将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色
③向某溶液中滴入盐酸酸化的BaCl2溶液产生白色沉淀,证明溶液中一定含有SO42-
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后按入水中,两者放出的氢气质量相等
A.只有② B.①②③ C.①③④ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
(1)软锰矿、闪锌矿与硫酸共热: MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O。
 (2)除去反应混合物中的不溶物
(2)除去反应混合物中的不溶物
(3)电解混合液MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
下列说法不正确的是 ( )
A.步骤⑴中每析出12.8g S沉淀共转移0.4mol电子
B.步骤⑴中ZnS的还原性大于MnSO4的还原性
C.电解时MnO2在阳极处产生
D.硫酸在生产中可循环使用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com