
科目: 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
右图为某种乙醇燃料电池示意图,工作时电子流方向如图所示,下列判断正确的是

A.X为氧气
B.电极A反应式:CH3CH2OH-12e-+3H2O=2CO2+12H+
C.电极材料活泼性:A>B
D.B电极附近溶液pH增大
查看答案和解析>>
科目: 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
某烃的一种同分异构体,核磁共振氢谱测得分子中只有一个吸收峰,则该烃的分子式不可能为
A.CH4 B.C5H12 C.C8H18 D.C9H20
查看答案和解析>>
科目: 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
在体积一定的密闭容器中,给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡:aA(g)+ bB(g) xC(g),符合图(1)所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图(2)中,Y轴是指
xC(g),符合图(1)所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图(2)中,Y轴是指

A.反应物A的百分含量 B.反应物B的平衡转化率
C.平衡混合气的密度 D.平衡混合气的总物质的量
查看答案和解析>>
科目: 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
常温下,以下各组离子在有关限定条件下溶液中一定能大量共存的是
A.由水电离产生的c(H+)=10-12 mol/L的溶液中:K+、Na+、Fe2+、NO3-
B.在c(H+)= mol/L的溶液中:K+、Fe3+、HCO3-、AlO2-
C.常温下, =1×10-12的溶液:K+、AlO2-、SO42-、Cl-
=1×10-12的溶液:K+、AlO2-、SO42-、Cl-
D. pH=13的溶液中:NH4+、Na+、CO32-、SO42-
查看答案和解析>>
科目: 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:推断题
有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A物质 18.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空: (1)A的相对分子质量为_______。 |
(2)A的核磁共振氢谱如图:
| (2)A中含有________种氢原子。 |
(3)另取A 18.0 g与足量的NaHCO3粉末反应,生成0.2 mol CO2,若与足量钠反应则生成0.2 mol H2。 | (3)写出一个A分子中所含官能团的名称和数量_____________。 |
(4)将此18.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8 g和26.4 g。 | (4)A的分子式为________。 |
(5)综上所述A的结构简式_____________________________。 | |
查看答案和解析>>
科目: 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:填空题
化学反应原理是中学化学学习的重要内容。请回答下列问题:
(1)下列判断正确的是______________。
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1 CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
则ΔH1﹤ΔH2
②H2(g)+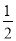 O2(g)===H2O(l) ΔH1 2H2(g)+O2(g)═2H2O(l) ΔH2
O2(g)===H2O(l) ΔH1 2H2(g)+O2(g)═2H2O(l) ΔH2
则ΔH1﹤ΔH2
③t ℃时,在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时反应放出的热量分别为Q1和Q2
则Q1﹤Q2
④CaCO3(s)===CaO(s)+CO2(g) ΔH1 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH2
则ΔH1﹤ΔH2
(2)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)
设计的原电池如图所示。

请回答下列问题:
①铜电极发生的电极反应为_____________________。
②溶液中Cu2+向________极移动。
(3)在一恒温、恒容密闭容器中充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g) + 3H2(g)  CH3OH (g) + H2O(g) △H=-49.0 kJ/mol
CH3OH (g) + H2O(g) △H=-49.0 kJ/mol
某种反应物和生成物的浓度随时间变化如图所示。
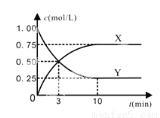
回答下列问题:
①Y的化学式是 。
②反应进行到3min时, v正 v逆(填“>”或“<”、“=”)。反应前3min,H2的平均反应速率,v(H2)= mol·L-1·min-1。
③能证明该反应达到化学平衡状态的依据是 。
A.容器内各气体的体积分数保持不变
B.混合气体密度不变
C.3v逆(CH3OH) =v正(H2)
D.混合气体的平均相对分子质量不变
E.CO2的转化率为70%
F.混合气体中CO2与H2的体积比为1﹕3
④上述温度下,反应CH3OH (g) + H2O(g)  CO2(g) + 3H2(g)的平衡常数K= (计算结果保留2位小数)。
CO2(g) + 3H2(g)的平衡常数K= (计算结果保留2位小数)。
⑤上述反应达到平衡后,往容器中同时加入0.1mol CO2和0.3mol H2O (g),此时平衡将 (填“向左”、“向右”或“不”)移动。
(4)室温时,向20 mL 0.1 mol/L的醋酸溶液中不断滴入0.1 mol/L的NaOH溶液,溶液的pH变化与所加NaOH溶液体积的关系如下图所示。下列有关溶液中离子、分子浓度大小关系的描述中正确的是____________。
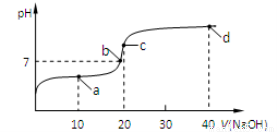
①.a点时:c(CH3COOH) >c(CH3COO-) > c(Na+) > c(H+) >c(OH-)
②.b点时:c(Na+)=c(CH3COO-) >c(H+) =c(OH-)
③.c点时:c(OH-)=c(CH3COOH)+c(H+)
④.d点时:c(Na+)> c(CH3COO-) > c(OH-) >c(H+)
查看答案和解析>>
科目: 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
以下关于合金的说法不正确的是
A.合金的硬度往往大于它的纯金属
B.合金的熔点高于它的成分金属
C.青铜是我国使用最早的合金
D.钢是使用量最大,用途最广的合金
查看答案和解析>>
科目: 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
以下氧化物既可以与酸反应,又可以与碱反应的是
A.FeO B.Fe2O3 C.Al2O3 D.Fe3O4
查看答案和解析>>
科目: 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
下列关于铝的叙述中,不正确的是
A.铝是地壳中含量最多的金属元素
B.铝单质能与盐酸溶液反应,又能与NaOH溶液反应
C.在常温下,铝不能和氧气反应
D.在化学反应中,铝容易失去电子,是还原剂
查看答案和解析>>
科目: 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
下列描述的一定是金属元素的是
A.易失去电子的物质 B.能与酸反应的物质
C.原子核内有11个质子的元素 D.原子的最外层只有一个电子的元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com