
科目: 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:选择题
关于硅的下列叙述中,正确的是
A.晶体硅与金刚石分子都是正四面体结构
B.硅酸盐都不溶于水
C.硅与酸、碱都不能发生反应
D.原硅酸和硅酸对应的酸酐都是二氧化硅
查看答案和解析>>
科目: 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:选择题
电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO的原理如图所示,下列说法不正确的是
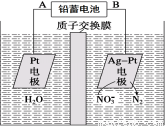
A.铅蓄电池的A极为正极,电极材料为PbO2
B.该电解池的总反应方程式为:2H2O + 4NO3-  2N2↑+ 5O2↑ + 4OH-
2N2↑+ 5O2↑ + 4OH-
C.该电解池的阴极反应式为:2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g
查看答案和解析>>
科目: 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:选择题
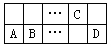
有A、B、C、D四种短周期元素在周期表中位置如图所示。已知:A2+与C原子的电子数相差2。下列推断不正确的是
…… | C | |||
A | B | …… | D |
A.A和D组成的化合物是弱电解质且水溶液呈酸性
B.与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应中常作催化剂
C.离子半径:C>A>B
D.B与C形成的化合物是冶金工业的一种原料
查看答案和解析>>
科目: 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:选择题
依据下列实验现象,得出的结论正确的是
操作 | 实验现象 | 结论 | |
A | 向NaBr溶液中加入氯水,再加入淀粉KI溶液 | 溶液变蓝 | 氧化性:Cl2>Br2>I2 |
B | 将铝片放入盐酸中 | 产生气泡的速率开始时较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 |
D | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
查看答案和解析>>
科目: 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:填空题
I.化工工业中常用乙苯脱氢的方法制备苯乙烯。
已知某温度下:
反应①:CO2 (g) +H2 (g)→CO(g) + H2O(g),ΔH = +41.2 kJ/mol;
反应②: 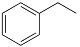 (g)→
(g)→ (g)+H2(g),ΔH= +117.6 kJ/mol;
(g)+H2(g),ΔH= +117.6 kJ/mol;
①②的化学反应平衡常数分别为K1、K2,
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式 ,该反应的化学平衡常数K= (用K1、K2表示)
(2)对于反应①,恒温恒容条件下,向密闭容器中加入2molCO2 和2molH2,当反应达到平衡后,以下说法正确的是
A.因为该反应是吸热反应,所以升高温度,正反应速率增大,逆反应速率减小;
B.若再加入1molCO2、1mol H2,平衡不移动;
C.若再加入CO2则平衡向正反应方向移动,CO的体积分数减小;
D.若充入He,平衡不移动,反应物和产物的浓度都不变;
(3)恒温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在下图中画出t1之后的正逆反应曲线,并作出标注。

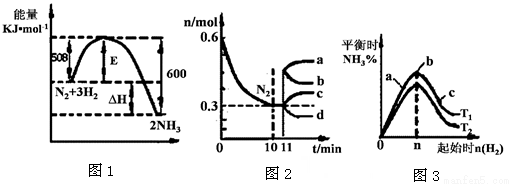
II.一定的条件下,合成氨反应为:N2(g)+3H2(g)  2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
(4)升高温度,该反应的平衡常数 (填“增大”或“减小”或“不变”)。
(5)由图2信息,计算10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
(6)图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
查看答案和解析>>
科目: 来源:2016届湖南省十校共同体高三上学期12月联考化学试卷(解析版) 题型:选择题
如图A~D四种物质均含有同一种元素,A可以是单质也可以是气态氢化物,D是该元素最高价氧化物对应的水化物,则A、B、C、D中共同含有的元素可能是
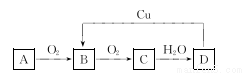
A.氯 B.铁 C.碳 D.氮
查看答案和解析>>
科目: 来源:2016届湖南省十校共同体高三上学期12月联考化学试卷(解析版) 题型:选择题
在溶液中加入足量Na2O2后仍能大量共存的离子组是
A. NH4+、Ba2+、Cl-、NO3- B.K+、AlO2-、C1-、SO42-
C. Ca2+、Mg2+、NO3-、HCO3- D.Na+、C1-、SO32-、SO42-
查看答案和解析>>
科目: 来源:2016届湖南省十校共同体高三上学期12月联考化学试卷(解析版) 题型:选择题
除虫菊酯是一种从植物除虫菊中提取出来的广谱杀虫剂,结构如图所示,下列描述正确的是
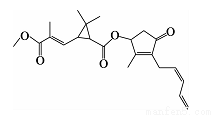
A.除虫菊酯属于芳香族化合物
B.除虫菊酯的分子式为C22H28O5
C.除虫菊酯在镍作催化剂下最多可与7 mol H2发生加成反应,与3 mol NaOH发生水解反应
D.除虫菊酯在酸性条件下发生水解后得到的产物均带有羧基
查看答案和解析>>
科目: 来源:2016届湖南省十校共同体高三上学期12月联考化学试卷(解析版) 题型:选择题
常温下,向20 mL某浓度的盐酸中逐滴加入0.1 mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示。

下列叙述正确的是
A.盐酸的物质的量浓度为l mol/L
B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-)
C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20
D.在点③所示溶液中:由水电离出的c(OH-)>l0-7mol/L
查看答案和解析>>
科目: 来源:2016届湖南省十校共同体高三上学期12月联考化学试卷(解析版) 题型:填空题
NH3是一种重要的化工产品。
(1)根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu)(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算Ar(Cu)。为此,提供的实验仪器及试剂如下(根据实验需要,装置可重复选择,加入的NH4 Cl与Ca(OH)2的量足以产生使CuO完全还原为N2的氨气)。

请回答下列问题:
①氨气还原炽热氧化铜的化学方程式为_______________;
②从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的字母表示)A→ ;
③在本实验中,若测得m( CuO) =ag,m(H2O)=b g,则Ar(Cu)= ;
④在本实验中,使测定结果Ar(Cu)偏大的是 (填字母);
A.CuO未完全起反应 B.CuO不干燥
C.CuO中混有不反应的杂质 D.NH4 Cl与Ca(OH)2混合物不干燥
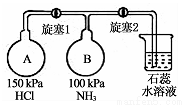
(2)按右图装置进行NH3性质实验。
①先打开旋塞1,B瓶中的现象是 原因是
②稳定后,关闭旋塞1,再打开旋塞2,B瓶中的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com