
科目: 来源:2015-2016学年辽宁省高二上12月月考化学试卷(解析版) 题型:填空题
结合下表回答下列问题(均为25℃时的数据)
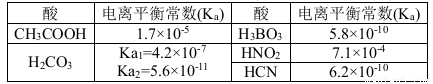
(1)上述五种酸中,酸性最强的是 (填化学式)。HCO3-的电离平衡常数表达式K= 。
(2)已知硼酸(H3BO3)与足量NaOH溶液发生酸碱中和反应的离子方程式为:H3BO3+ OH-= B(OH)4-, 则硼酸为 元酸,硼酸的电离方程式为 。
(3)常温下,0.01 mol·L-1的HNO2 溶液加水稀释的过程中,下列各项数据增大的是 (填代号)。
①c(H+ ) ②c (NO2- )/ c(H+) ③Ka(HNO2)
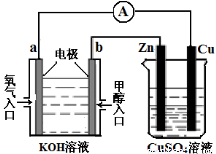
④c(H+ )/ c(HNO2) ⑤c(OH -) ⑥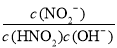
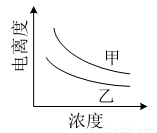
(4)右图描述的是醋酸与HNO2 在水中的电离度与浓度关系,其中反映醋酸的是曲线 (填“甲”或“乙”,已知:电离度=已电离的溶质分子数/原有溶质分子总数) 。
(5)根据表中提供的数据可知,在溶液中能大量共存的微粒组是 (填代号)。
A. H2CO3、HCO3-、 CH3COO-、CN- B. HCO3-、 CH3COOH、CN- 、CO32—
C. HCN、 HCO3-、CN- 、CO32— D. HCN、 HCO3-、CH3COO-、CN-
(6)设计一个现象明显、操作简便的实验方案证明HNO2酸性强于碳酸(不用叙述仪器和具体操作)。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:选择题
已知: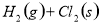
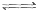
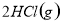 △
△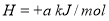
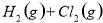
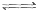
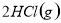 △
△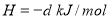
 ,且
,且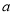 、
、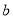 、
、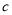 、
、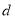 均大于零,则下列说法正确的是
均大于零,则下列说法正确的是
A.断开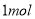
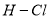 键所需的能量为
键所需的能量为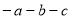
B.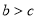 ,则氢分子具有的能量高于氯气分子具有的能量
,则氢分子具有的能量高于氯气分子具有的能量
C.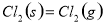 △
△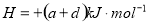
D.向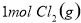 中通入
中通入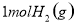 ,发生反应时放热
,发生反应时放热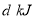
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:选择题
一定温度下,反应2SO2 + O2 2SO3,达到平衡时,n(SO2):n(O2):n(SO3) = 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是
2SO3,达到平衡时,n(SO2):n(O2):n(SO3) = 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是
A.0.4mol B.0.6mol C.0.8mol D.1.2mol
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:选择题
下列事实中一定不能证明CH3COOH是弱电解质的是
①常温下某CH3COONa溶液的pH=8
②用CH3COOH溶液做导电实验,灯泡很暗
③等pH、等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多
④0.1 mol·L-1 CH3COOH溶液的pH=2.1
⑤CH3COONa和H3PO4反应,生成CH3COOH
⑥0.1 mol·L-1的CH3COOH溶液稀释100倍,pH<3
A.② B.②⑤ C.①③⑤ D.③④⑤⑥
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:选择题
已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15。在AB2、AC均为饱和的混合液中,测得c(B-)=1.6×10-3 mol·L-1,则溶液中c(C2-)为
A. 7.3×10-13 mol·L-1 B. 1.8×10-13 mol·L-1
C.2.3 mol·L-1 D.3.7 mol·L-1
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:填空题
在密闭容器中投入一定量的A和B发生反应:m A(g)+n B(g)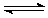 p C(g)+q D(g)。
p C(g)+q D(g)。
(1)若开始时加入A物质m mol,B物质n mol,则达到平衡时 A、B的转化率____________.(填“相等”或“不等”)
(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间T的关系如图3所示。则T1(填“>”、“<”或“=”) T2,该反应的正反应的△H(填“>”、“<”或“=”) 0。

(3)一定条件下,从正反应开始达到化学平衡过程中,混合气体的平均相对分子质量随时间的变化如图4所示,测得达到平衡时A、B、C、D的物质的量均为1 mol。
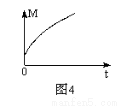
①若在恒温恒容的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的平均相对分子质量(填“增大”、“减小”、“不变”或“无法确定”)______ 。
②若恒温恒压的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的密度(填“增大”、“减小”、“不变”或“无法确定”) 。
(4)若该反应的逆反应速率与时间的关系如下图所示:
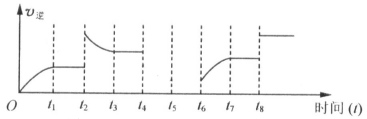
可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了条件,试判断t2时改变的条件是 。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:填空题
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g)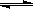 CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数
CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数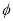 (CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)
(CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)

(2)若在230℃时,平衡常数K=1。若其它条件不变,将温度升高到500℃时,达到平衡时,K 1。
(3)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的 倍。
(4)利用甲醇燃料电池设计如图所示的装置:
①则该装置中b为 极。
②当铜片的质量变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为 L。
(5)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)== C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l)== C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方为 。
查看答案和解析>>
科目: 来源:2015-2016学年江西省高二上12月月考化学试卷(解析版) 题型:选择题
目前,科学家正在研究开发一种高能电池——钠硫电池,它以熔融钠、硫为两极,以导电的β—Al2O3陶瓷作固体电解质,反应式如下:2Na+xS  Na2Sx,以下说法正确的是
Na2Sx,以下说法正确的是
A.放电时,Na作正极,S极发生还原反应
B.充电时,钠极与外电源的正极相连
C.放电时,阳极发生的反应为:S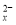 -2e=xS
-2e=xS
D.若用此电池电解AgNO3溶液,当阳极产生标准状况下的气体1.12L时,消耗的金属钠为4.6g
查看答案和解析>>
科目: 来源:2015-2016学年江西省高二上12月月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子,在所给的条件下,一定能够大量共存的是
A、在c(H+)/c(OH-)=1×1012的溶液中:Fe2+、Mg2+、CO32-、NO3-
B、在由水电离出的c(H+)=1×10-12mol/L的溶液中:HCO3-、Al3+、NH4+、ClO-
C、在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl-、AlO2-、CO32-
D、在AlCl3溶液中:K+、NO3-、S2-、Na+
查看答案和解析>>
科目: 来源:2015-2016学年江西省高二上12月月考化学试卷(解析版) 题型:选择题
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36.常温时下列有关说法正确的是
A.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强
B.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35 mol/L
C.因为H2SO4是强酸,所以反应:CuSO4+H2S===CuS↓+H2SO4不能发生
D.除去工业废水中的Cu2+可以选用FeS作沉淀剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com