
科目: 来源:2015-2016学年四川省雅安市高二上学期期中测试化学试卷(解析版) 题型:选择题
下列图式表示正确的是
A.二氧化碳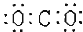
B.次氯酸的结构式 H-Cl-O
C.铝离子的结构示意图
D.基态碳原子的价电子排布图为
查看答案和解析>>
科目: 来源:2015-2016学年四川省雅安市高二上学期期中测试化学试卷(解析版) 题型:选择题
下列离子方程式中书写正确的是
A.氯化铝溶液中加入足量的氨水:Al3++3NH3·H2O= Al(OH)3 ↓+3NH4+
B.水玻璃中加入稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
C.二氧化硅与苛性钠溶液反应:SiO2+OH-=SiO32-+H2O
D.氧化铝与NaOH溶液反应:Al2O3+10OH-= 2[Al(OH)4]-+H2↑
查看答案和解析>>
科目: 来源:2015-2016学年四川省雅安市高二上学期期中测试化学试卷(解析版) 题型:填空题
今有aX、bY、cZ三种元素。已知:①各原子序数a、b、c均小于20,且a+b+c=25; ②元素Y的原子价电子构型为ns2npn+2; ③X和Y在不同条件下可形成X2Y和X2Y2两种化合物,Y和Z在不同条件下可形成ZY和ZY2两种化合物; ④Z的硫化物的相对分子质量与Z氯化物的相对分子质量之比为38︰77。回答下列问题:
(1)X: (写元素名称);Z的价电子排布图为: 。
(2)X2Y2的电子式 ,属于 化合物(填“离子”或“共价”)。
(3)Z的硫化物的VSEPR模型为 ,分子空间构型为 ;Z的氯化物的VSEPR模型和分子空间构型分别是 、 ,其中Z原子分别以 杂化轨道成键,根据原子轨道成键方式分,Z的硫化物分子中含有的键的种类及数目是 、 。
查看答案和解析>>
科目: 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
过量的锌粉与10 mL 浓度为1 mol ·L-1的盐酸反应,若加入适量的下列溶液,能减慢反应速率但不影响氢气生成量的是
A.CH3COOH B.CuSO4 C.K2SO4 D.NaHCO3
查看答案和解析>>
科目: 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列事实能说明H2SO3不是强电解质的是
① 0.05 mol/L H2SO3 溶液的pH>1 , ② 常温下Na2SO3溶液的pH>7 ,
③ H2SO3不稳定,易分解, ④ H2SO3能与碳酸钠反应制CO2 ,
⑤ H2SO3能和水以任意比例互溶, ⑥ 1mol H2SO3能够消耗2 mol NaOH
A.①②⑤ B.①②④ C.①②③⑤ D.①②
查看答案和解析>>
科目: 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
一定条件下反应2AB(g)  A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内三种气体AB、A2、B2共存
C.容器中各组分的体积分数不随时间变化
D.AB的消耗速率等于A2的消耗速率
查看答案和解析>>
科目: 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列措施或事实不能用勒沙特列原理解释的是
A.在合成氨的反应中,增大压强有利于氨的合成
B.H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深
C.新制的氯水在光照下颜色变浅
D.氯气可以用排饱和食盐水的方法收集(Cl2+ H2O HCl+ HClO)
HCl+ HClO)
查看答案和解析>>
科目: 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:填空题
甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。
(1)CO2可用于合成二甲醚(CH3OCH3),有关反应的热化学方程式如下:
CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH = -49.0kJ·mol-1,
2CH3OH(g) = CH3OCH3(g)+ H2O(g) ΔH =-23.5kJ·mol-1,
则CO2与H2反应合成二甲醚的热化学方程式为 。
(2)若反应2CH3OH(g)  CH3OCH3(g) + H2O(g)在某温度下的化学平衡常数为400,此温度下,在密闭容器中加入一定量甲醇,反应进行到某时刻,测得各物质的浓度如表所示:
CH3OCH3(g) + H2O(g)在某温度下的化学平衡常数为400,此温度下,在密闭容器中加入一定量甲醇,反应进行到某时刻,测得各物质的浓度如表所示:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度(mol·L-1) | 0.44 | 0.60 | 0.60 |
①写出该反应的平衡常数表达式:K= 。
②比较该时刻正、逆反应速率的大小:v(正) v(逆)(填“>”、“<”或“=”)
③若加入甲醇后经 10 min 反应达到平衡,则平衡后c(CH3OH)= ,该时间内反应速率v(CH3OCH3)= 。
(3)工业上合成甲醇的反应:CO(g)+2H2(g) CH3OH(g) ΔH =-90.8kJ·mol-1,若在温度相同、容积均为2L的3个容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时如下:
CH3OH(g) ΔH =-90.8kJ·mol-1,若在温度相同、容积均为2L的3个容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molCO、2 mol H2 | 1 mol CH3OH | 2 mol CO、4 mol H2 |
CH3OH的浓度(mol/L) | c1=0.25 | c2 | c3 |
反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
平衡常数 | K1 | K2 | K3 |
反应物转化率 | α1 | α2 | α3 |
①下列不能说明该反应在恒温恒容条件下已达化学平衡状态的是 。
A. v正(H2)= 2v逆(CH3OH) B. n(CO)﹕n(H2)﹕n(CH3OH)=1﹕2 : 1
C. 混合气体的密度不变 D. 混合气体的平均相对分子质量不变
E. 容器的压强不变
②下列说法正确的是 。
A. c1= c2 B. Q1= Q2 C. K1= K2 D. α2+α3 < 100%
③如图表示该反应的反应速率v和时间t的关系图:
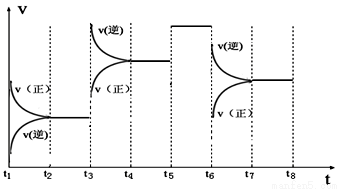
各阶段的平衡常数如下表所示:
t2~t3 | t4~t5 | t5~t6 | t7~t8 |
K4 | K5 | K6 | K7 |
K4、K5、K6、K7之间的关系为 (填“>”、“<”或“=”)。反应物的转化率最大的一段时间是 。
查看答案和解析>>
科目: 来源:2015-2016学年广东省普宁市高一上学期第三次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1.8g的NH4+ 离子中含有的电子数0.1NA
B.25℃,1.01×105Pa,64gSO2中含有的原子数为3 NA
C.在常温常压下,11.2LCl2含有的分子数为0.5 NA
D.标准状况下,11.2LH2O中含有的分子数目为0.5NA
查看答案和解析>>
科目: 来源:2015-2016学年广东省普宁市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列图示装置的实验中,操作正确的是
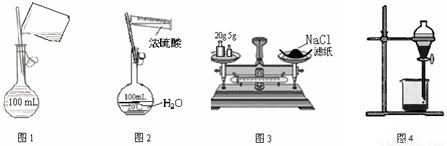
A.图1配制250mL0.10mol·L-1盐酸 B.图2稀释浓硫酸
C.图3称量氯化钠固体 D.图4CCl4萃取碘水的分液操作
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com