
科目: 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:选择题
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是
A.常温常压下,N2和O2混合气体22.4 L所含的分子数少于6.02×1023
B.1 L l mol/LFeBr2溶液与l mol氯气反应时转移的电子数为3NA
C.标准状况下,11.2 L HF 所含的分子数约为3.01×1023
D.0.5 mol/L硫酸钠溶液中含有溶质离子总数为1. 5NA
查看答案和解析>>
科目: 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:选择题
SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
下列有关说法错误的是
A.氧化性:Cr2O72->Fe3+>SO2
B.K2Cr2O7能将Na2SO3氧化成Na2SO4
C.每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA
D.若有6.72 L SO2(标准状况)参加反应,则最终消耗0.2 mol K2Cr2O7
查看答案和解析>>
科目: 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:选择题
已知电离平衡常数:H2CO3>HClO>HCO3-,下列有关叙述中,正确的是
①若KI溶液中混有Br-,加入足量FeCl3溶液,用CCl4萃取后,取无色的水层并加入AgNO3溶液,有淡黄色沉淀生成。
②向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2===2Fe3++2Cl-
③向NaClO溶液中通入少量二氧化碳的离子反应方程式:2ClO-+CO2+H2O===2HClO+CO32—
④海水提溴过程中,用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为
3Br2+6CO32-+3H2O=5Br-+ BrO3-+6HCO3-
A.② ④ B.① ③ C.② ③ D.① ④
查看答案和解析>>
科目: 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:选择题
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是
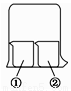
①中的物质 | ②中的物质 | 预测①的现象 | |
A | 淀粉?KI溶液 | 浓硝酸 | 无明显变化 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
查看答案和解析>>
科目: 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:填空题
硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个有一个奇迹。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方程式 。
(2)一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的工艺主要流程如下:
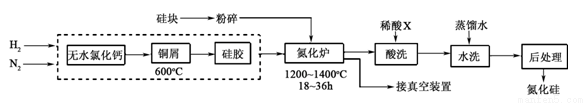
①净化N2和H2时,铜屑的作用是: ;硅胶的作用是 。
②在氮化炉中3SiO2(s)+2N2(g)=Si3N4(s) △H=-727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度 ;体系中要通入适量的氢气是为了 。
③X可能是 (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(3)工业上可以通过如下图所示的流程制取纯硅:
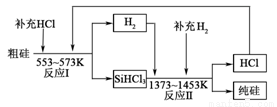
①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,写出该反应的化学方程式 。
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
查看答案和解析>>
科目: 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:填空题
某种盐可表示为[xFeSO4·y(NH4)2SO4·6H2O](其摩尔质量为392g·mol-1),可用作标定重铬酸钾、高锰酸钾等溶液的标准物质,也可用于冶金、电镀。为测定其组成,进行下列实验:
①取一定质量的上述盐样品,准确配制100mL的溶液X;
②量取20.00mL的溶液X,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,烘干至恒重,得到白色固体Y 4.660g
③另取20.00mL的X溶液,滴加适量硫酸,用0.1000mol·L-1的KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液20.00mL。
(1)在20.00mL试样溶液中c(SO42-)= mol·L-1,n(Fe2+)= mol;
(2)该盐的化学式为 。
查看答案和解析>>
科目: 来源:2016届重庆市高三11月月考理科综合化学试卷(解析版) 题型:选择题
在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是
A.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+
B.在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、H+、Fe2+
C.在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3、K2CO3
D.在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32-
查看答案和解析>>
科目: 来源:2016届重庆市高三11月月考理科综合化学试卷(解析版) 题型:选择题
能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式
① | H2(g)+ | |||||||
② | 2H2(g)+ O2(g)= 2H2O(l) △H =﹣572kJ/mol; | |||||||
③ | C(s)+ | |||||||
④ | C(s)+ O2(g)= CO2(g) △H =﹣393.5kJ/moL; | |||||||
⑤ | CO2(g)+ 2H2O(g)= CH4(g)+ 2O2(g)△H = + 802kJ/moL | |||||||
化学键 | O=O | C-C | H-H | O-O | C-O | O-H | C-H | |
键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 | |
则下列说法正确的是
A.H2燃烧热的热化学方程式为H2(g)+ O2(g)= H2O(g) △H =﹣242kJ /mol
O2(g)= H2O(g) △H =﹣242kJ /mol
B.热化学方程式:C(s)+ H2O(g) H2(g)+ CO(g) △H = + 175.5 kJ/moL
H2(g)+ CO(g) △H = + 175.5 kJ/moL
C.CH4的燃烧热△H =— 802 kJ/moL
D.估算出C=O键能为800kJ/moL
查看答案和解析>>
科目: 来源:2016届重庆市高三11月月考理科综合化学试卷(解析版) 题型:推断题
如下对甲、乙、丙三种物质的说明:

(1)甲中含氧官能团的名称为 。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应Ⅰ的反应类型为 ,反应Ⅱ的化学方程式为 (注明反应条件)。
(3)已知:

由乙制丙的一种合成路线图如下(A﹏F均为有机物,图中Mr表示相对分子质量):

① 下列物质不能与C反应的是 (选填序号)
a. 金属钠 b.HBr c.Na2CO3溶液 d. 乙酸
② 写出F的结构简式
③ D有多种同分异构体,其中一种既能发生银镜反应又能发生水解反应的结构简式 其
④综上分析,丙的结构简式为
查看答案和解析>>
科目: 来源:2015-2016学年广东省高一上学期月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com