
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.无色溶液中: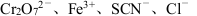
B.能使石蕊呈蓝色的溶液中: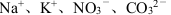
C. c (H+ )/ c(OH -)=1012 的溶液中: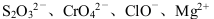
D.水电离的c (H)=10-12 mol·L-1 的溶液中: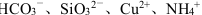
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
有等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
A.V3=V2=V1 B.V3>V2=V1 C.V1=V2>V3 D.V3>V2>V1
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
(原创)如图表示不同温度下水溶液中c(H+)与c(OH-)的关系,下列判断正确的是( )
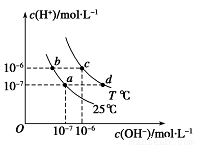
A.两条曲线上任意点均有c (H+) ×c (OH-)=Kw
B.T<25℃
C.b点和c点pH均为6,溶液呈酸性
D.只采用升温的方式,可由a点变成d点
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
常温下,向纯水中加入NaOH使溶液的pH为11,则由NaOH电离出的OH 离子浓度和水电离出的OH离子浓度之比为 ( )
A.1:1 B.108 :1 C.5×109 :1 D.1010 :1
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
用0.1000 mol·L-1NaOH溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是( )
A.盛装待测液的锥形瓶用蒸馏水洗过,没用待测液润洗
B.酸式滴定管在使用前未用待测液盐酸润洗
C.滴定前碱式滴定管尖嘴中有气泡,滴定后气泡消失
D.滴定前读数平视,滴定终点读数时俯视碱式滴定管的刻度
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
(原创)液氨与纯水类似,也存在微弱的电离:NH3+ NH3  NH4+ +NH2- ,下列说法不正确的是( )
NH4+ +NH2- ,下列说法不正确的是( )
A.只要不加入其他物质,液氨中c(NH4+ )总是等于c(NH2- )
B.一定温度下, c(NH4+ )×c(NH2- )为常数
C.其他条件不变,增加液氨的量,电离平衡正向移动
D.维持温度不变,向液氨中加入少量NH4Cl固体,c(NH2-)将减少
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:填空题
某实验小组依据反应 设计如图1原电池,探究pH对AsO4 氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
设计如图1原电池,探究pH对AsO4 氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
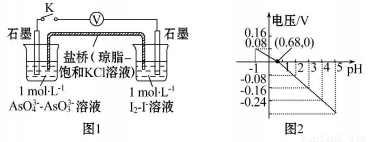
A.调节pH可以改变反应的方向
B. pH=0.68时,反应处于平衡状态
C.pH=5时, 负极电极反应式为2I--2e -= I2
D.pH>0.68时,氧化性I2>AsO43-
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
t℃时,某NaOH稀溶液中,c(H+ )=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=13, 则在该温度下,将100 mL0.10 mol·L-1的稀硫酸与100 mL0.40 mol·L-1的NaOH溶液混合后,溶液的pH为( )(已知:忽略溶液混合时体积的变化;lg2=0.30;lg3=0.48)
A.12.00 B.11.82 C.11.70 D.11.52
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:填空题
(原创)I.现有以下物质:①铁 ②稀硝酸 ③明矾 ④液氨 ⑤冰醋酸 ⑥蔗糖溶液 ⑦无水乙醇 ⑧熔融态的氢氧化钠⑨硫酸钡晶体 ⑩三氧化硫气体,回答下列问题(用相应物质序号填写):
(1)可以导电的有 。(2)属于强电解质的有 。
II. A、B、C、D四种溶液分别是氢氧化钡溶液、氨水、醋酸溶液、盐酸中的一种。
已知同浓度的四种溶液:①加入大小完全相同的锌粒,仅A、C中放出气体,且开始时A中冒气泡的速度快;②相同条件下,取B、D溶液进行导电性实验,发现导电能力最差的是D。回答下列问题:
(3)D溶液为 ;同浓度的四种溶液中,pH值最大的是 (填化学式) 溶液。
(4)pH值和体积均相同的A和C溶液,分别与足量且大小完全相同的锌粒反应,开始时的反应速率v(A) v(C) (填“>”、“<”或“=”,下同),最终产生气体的物质的量n(A) n(C)。
(5)等体积等浓度的氨水和盐酸混合后,所得溶液呈 (填“酸性”、“碱性”或“中性”),用离子方程式解释其原因 。
(6)0.1mol/L氨水中除水分子以外的粒子有 (填化学式)。
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:填空题
(原创)结合下表回答下列问题(均为25℃时的数据)
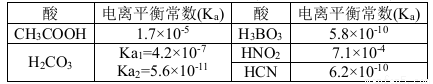
(1)上述五种酸中,酸性最强的是 (填化学式)。HCO3-的电离平衡常数表达式K= 。
(2)已知硼酸(H3BO3)与足量NaOH溶液发生酸碱中和反应的离子方程式为: HBO3+ OH-=B(OH)4-,则硼酸为 元酸,硼酸的电离方程式为 。
(3)常温下,0.01 mol·L-1的HNO2溶液加水稀释的过程中,下列各项数据增大的是 (填代号)。
①c(H+ ) ②c(NO2- )/ c(H+) ③Ka(HNO2)
④c(H+ )/ c(HNO2) ⑤c(OH-) ⑥ 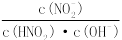
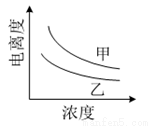
(4)右图描述的是醋酸与HNO2在水中的电离度与浓度关系, 其中反映醋酸的是曲线 (填“甲”或“乙”,已知:电离度=已电离的溶质分子数/原有溶质分子总数) 。
(5)根据表中提供的数据可知,在溶液中能大量共存的微粒组是 (填代号)。

(6)设计一个现象明显、操作简便的实验方案证明HNO2酸性强于碳酸(不用叙述仪器和具体操作)___________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com