
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
(原创)下列说法不正确的是( )
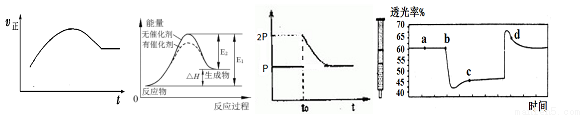
甲 乙 丙 丁
A.绝热恒容密闭容器中通入A和B,发生反应:2A (g)+B (g)  2C(g),图甲为其正反应速率随时间变化的示意图,则该反应为放热反应。
2C(g),图甲为其正反应速率随时间变化的示意图,则该反应为放热反应。
B.催化剂能降低反应的活化能,提高活化分子的百分含量,从而加快化学反应速率。图乙显示的是催化反应与无催化反应过程中的能量关系。
C.将BaO2放入密闭真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡时体系压强为P,保持温度不变,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡,体系压强变化如图丙所示。
2BaO(s)+O2(g)达到平衡时体系压强为P,保持温度不变,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡,体系压强变化如图丙所示。
D.将一定量的NO2充入针筒中后封口,发生反应2NO2 (g) N2O4(g),图丁[表示在拉伸和压缩针筒活塞的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。则c点与a点相比,c(NO2)增大,c(N2O4)增大。
N2O4(g),图丁[表示在拉伸和压缩针筒活塞的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。则c点与a点相比,c(NO2)增大,c(N2O4)增大。
查看答案和解析>>
科目: 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:填空题
(原创)NH3是一种重要的化工产品,可用于生产尿素 [CO(NH2)2]、处理烟气等。
Ⅰ.工业上合成尿素的反应:
2NH3(g)+CO2(g) CO(NH2)2 (l) + H2O (g) ΔH
CO(NH2)2 (l) + H2O (g) ΔH
(1) 已知合成尿素的反应分两步进行:
2NH3(g)+CO2(g) NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1
NH2COONH4(s)  CO(NH2)2(l)+ H2O (g) ΔH2
CO(NH2)2(l)+ H2O (g) ΔH2
其能量变化曲线如图1所示,则△H、△H1和△H2由小到大的顺序为__________。
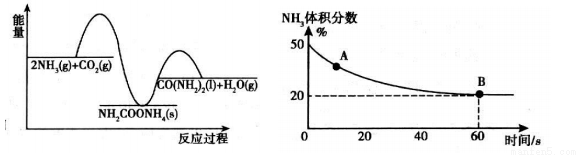
图1 图2
(2) 某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应:2NH3(g)+CO2(g)  CO(NH2)2 (l) + H2O (g) ,反应过程中混合气体中NH3的体积分数如图2所示。
CO(NH2)2 (l) + H2O (g) ,反应过程中混合气体中NH3的体积分数如图2所示。
①A点的逆反应速率v逆(CO2)______B点的正反应速率v正(CO2)。 (填“>”、“<”或“=”)
②下列能说明该反应达到平衡状态的是________________(填代号)。
a. NH3、CO2、H2O的分子数之比为2:1:1 b.体系的压强保持不变
c.单位时间内消耗1mol CO2同时生成2mol NH3 d.2v正(NH3) =v逆(H2O)
③对于有气体参与的反应,平衡常数Kp可用气体组分(B)的平衡分压p(B)代替该气体的物质的量浓度c(B)。实验测得体系平衡时的压强为10MPa,列式计算该反应的平衡常数Kp=_______ (提示:写出Kp的表达式再代入数据进行计算,分压=总压×体积分数)。
④L(L1、L2),X可分别代表压强或温度。右图表示L一定时,该反应CO2 (g)的平衡转化率随X的变化关系。
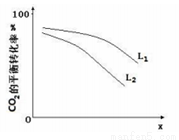
X代表的物理量为__________。判断L1、L2的大小关系,并简述理由: 。
Ⅱ.烟气中的NOx必须脱除(即脱硝)后才能排放:
(3)下图是一种用NH3脱除烟气中 NO的原理。该脱硝反应中,氧化剂是 (填化学式) 。
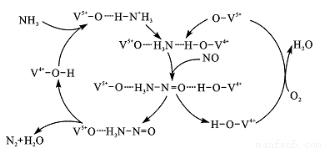
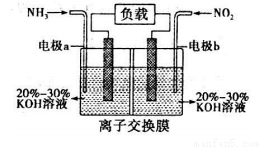
(4)利用反应8NH3+6NO2═7N2+12H2O构成原电池,也能消除烟气的排放,同时还能充分利用化学能,装置如图所示。则电极b为______极;a电极的电极反应式为 。
查看答案和解析>>
科目: 来源:2015-2016学年陕西省高二上期中质检化学试卷(解析版) 题型:选择题
已知H+(ag)+OH-(ag)=H2O(l) △H= -57.3kJ•mol-1。现有以下四个化学反应方程式:
①H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l)
②H2SO4(aq)+Ba(OH)2(aq)═BaSO4(s)+2H2O(l);
③HCl(aq)+NH3•H2O(aq)═NH4Cl(aq)+H2O(l);
④CH3COOH(aq)+NH3•H2O(aq)═CH3COONH4(aq)+H2O(l);其中反应热为△H=-57.3kJ•mol-1的是
A.①和③ B.③ C.④ D.以上都不对
查看答案和解析>>
科目: 来源:2015-2016学年陕西省高二上期中质检化学试卷(解析版) 题型:选择题
对于反应N2+O2 2NO,在密闭容器中进行,下列条件能使该反应的逆反应速率加快的是
2NO,在密闭容器中进行,下列条件能使该反应的逆反应速率加快的是
A.缩小体积使压强增大
B.压强不变充入He使体积增大
C.体积不变充入He使压强增大
D.压强不变充入N2使体积增大
查看答案和解析>>
科目: 来源:2015-2016学年陕西省高二上期中质检化学试卷(解析版) 题型:选择题
一定温度下,浓度均为1 mol•L-1的A2和B2两种气体,在密闭容器中反应生成气体C,反应达到平衡后,测得:c(A2)=0.58 mol•L-1,c(B2)=0.16 mol•L-1,c(C)=0.84mol•L-1,则该反应的正确表达式为:
A.2A2+B2 2A2B B.A2+B2
2A2B B.A2+B2 2AB
2AB
C.A2+B2 A2B2 D.A2+2B2
A2B2 D.A2+2B2 2AB2
2AB2
查看答案和解析>>
科目: 来源:2015-2016学年陕西省高二上期中质检化学试卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行可逆反应:X(g)+Y(g) Z(g)+W(s) △H>0,下列叙述正确的是
Z(g)+W(s) △H>0,下列叙述正确的是
A.当容器中气体密度不变时,反应达到平衡
B.加入少量W,逆反应速率增大
C.升高温度,Y的百分含量增加
D.平衡后加入X,上述反应的△H增大
查看答案和解析>>
科目: 来源:2015-2016学年陕西省高二上期中质检化学试卷(解析版) 题型:填空题
25℃、101kPa时,一些物质的燃烧热为:
化学式 | CO(g) | H2(g) | CH3OH(l) |
△H/( kJ•mol-1) | -283.0 | -285.8 | -726.5 |
请回答下列问题:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:_____________________;
(2)根据盖斯定律完成反应的热化学方程式:CO(g)+2H2(g)═CH3OH(l)△H=_____________。
查看答案和解析>>
科目: 来源:2015-2016学年陕西省高二上期中质检化学试卷(解析版) 题型:简答题
一定温度下,在容积固定的VL密闭容器里加入nmolA,2nmolB,发生反应A (g)+2B (g) 2C (g) △H<0,反应达到平衡后测得平衡常数为K,此时A的转化率为x.
2C (g) △H<0,反应达到平衡后测得平衡常数为K,此时A的转化率为x.
(1)K和x的关系满足K=_____________,在保证A浓度不变的情况下,增大容器的体积,平衡______(填字母)。A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(2)若该反应的逆反应速率与时间的关系如图所示:
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时_____________;t8时_____________;
②t2时平衡向___________(填“正反应”或“逆反应”)方向移动;
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
查看答案和解析>>
科目: 来源:2015-2016学年山东省高一上期中测试化学试卷(解析版) 题型:选择题
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )
A.常温常压下,1.6g臭氧中含有6.02×1022个氧原子
B.标准状况下,2.24 L水中含有6.02×1022个水分子
C.2.24 L氨气分子中含6.02×1023个电子
D.2.4 g金属镁变为镁离子时失去6.02×1022个电子
查看答案和解析>>
科目: 来源:2015-2016学年山东省高一上期中测试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.5.4gAl与足量的氢氧化钠溶液反应应失去的电子数为0.2NA
B.1L1mol/L的CaCl2溶液中含Cl-的数目为2NA
C.在25℃、1.01×105Pa的条件下,2.24LH2中含有的分子数为0.1NA
D.在标准状况下,11.2L某气体的质量为22g,则该气体的相对分子质量是44g/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com