
科目: 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:选择题
常温下,某H2CO3溶液的pH约为5.5,c(CO32-)约为5×10-11 mol•L-1,该溶液中浓度最小的离子是( )
A.CO32- B.HCO3- C.H+ D.OH-
查看答案和解析>>
科目: 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:选择题
下列物质既能通过化合反应,又能通过复分解反应生成的是( )
①Fe(OH)3 ②Fe(NO3)2 ③NaHCO3 ④Al2S3 ⑤NH4Cl ⑥NaOH
A.④除外都可以 B.除②④外都可以 C.只有①⑤⑥可以 D.全部都可以
查看答案和解析>>
科目: 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:选择题
溶液中含有较高浓度的NH4+、F-、HSO3-、K+等离子,向其中加入少量NaClO固体后,溶液中离子数目肯定增加的是( )
A.F- B.ClO- C.HSO3- D.NH4+
查看答案和解析>>
科目: 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:选择题
O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀毒消毒能力。常温常压下发生反应如下:反应①O3?O2+[O]△H>0 平衡常数为K1;
反应②[O]+O3=2O2△H<0 平衡常数为K2;
总反应:2O3=3O2△H<0 平衡常数为K
下列叙述正确的是( )
A.升高温度,K增大
B.K=K1+K2
C.压强增大,K2减小
D.适当升温,可提高消毒效率
查看答案和解析>>
科目: 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:选择题
甲、乙、丙、丁4种化合物均含有2种或3种元素,分子中均含有18个电子。甲是气态氢化物。在水中分步电离出两种阴离子。下列推断合理的是( )
A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应
B.乙和甲中同种元素的质量分数相等,则乙中含有化合价为-1的元素
C.丙与氧气的摩尔质量相同,则丙一定仅由两种元素组成
D.丁中含有第二周期ⅣA族元素,则丁一定是甲烷的同系物
查看答案和解析>>
科目: 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:实验题
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
CO(NH2)+2NaOH+NaClO═Na2CO3+N2H4•H2O+NaCl
NaClO过量时,易发生N2H4•H2O+2NaClO═N2↑+2NaCl+3H2O
实验一:制备NaClO溶液.(实验装置如图1所示)
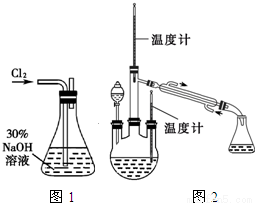
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有______________(填标号);
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的化学方程式是______________;
实验二:制取水合肼.(实验装置如图2所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(已知:N2H4•H2O+2NaClO═N2↑+3H2O+2NaCl)
(3)分液漏斗中的溶液是_______(填标号);
A.CO(NH2)2溶液
B.NaOH和NaClO混合溶液
选择的理由是______________;
实验三:测定馏分中肼含量
称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL,用0.1000mol•L-1的I2溶液滴定.滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4•H2O+2I2═N2↑+4HI+H2O)
(4)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,用离子方程式解释其原因______________;
(5)实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4•H2O)的质量分数为___________;
查看答案和解析>>
科目: 来源:2016届河北省高三上一轮收官考试理综化学试卷(解析版) 题型:选择题
下列实验装置能达到相关实验目的的是( )
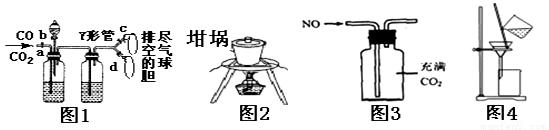
A.图1可用于分离收集CO和CO2
B.图2可用于从食盐水中提取NaCl晶体
C.图3用于收集NO
D.图4用于氢氧化铁胶体和硫酸钠溶液的分离
查看答案和解析>>
科目: 来源:2016届河北省高三上一轮收官考试理综化学试卷(解析版) 题型:填空题
铅及其化合物在工业生产生活中都具有非常广泛的用途。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)↑H=a kJ/mol
PbS(s)+2PbO(s)=3Pb(s)+SO2(g)↑H=b kJ•mol-1
PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)↑H=c kJ•mol-1
反应3PbS(s)+6O2(g)=3PbSO4(s)△H=_____________kJ•mol-1(用含a,b,c的代数式表示)。
(2)还原法炼铅,包含反应PbO(s)+CO(g) Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
温度 | 300 | 727 | 1227 |
lgK | 6.17 | 2.87 | 1.24 |
①该还原反应的△H____0(选填:“>”“<”“=”)。
②当lgK=1且起始时只通入CO(PbO足量),达平衡时,混合气体中CO的体积分数为_______。
(3)引爆导弹、核武器的工作电源通常Ca/PbSO4热电池,其装置如图所示,该电池正极的电极反应式为_______。

(4)PbI2:可用于人工降雨.取一定量的PbI2固体,用蒸馏水配制成t℃饱和溶液,准确移取25.00mLPbI2饱和溶液分次加入阳离子交换树脂RH+(发生:2RH++PbI2=R2Pb+2H++2I-),用250ml洁净的锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并盛放到锥形瓶中(如图).加入酚酞指示剂,用0.0025mol•L-1NaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL.可计算出t℃时PbI2 Ksp为_______。

(5)铅易造成环境污染,水溶液中的铅存在形态主要有6种,它们与pH关系如图1所示,含铅废水用活性炭进行处理,铅的去除率与pH关系如图2所示.

①常温下,pH=6→7时,铅形态间转化的离子方程式为____________________。
②用活性炭处理,铅的去除率较高时,铅主要应该处于________(填铅的一种形态的化学式)形态.
查看答案和解析>>
科目: 来源:2016届河北省高三上一轮收官考试理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】
X、Y、Z、L四种元素分别位于周期表中三个紧相邻的周期且原子序数依次增大,它们相关信息如下:X元素原子的价电子构型为nsnnp2n,Y和Z位于同一周期,最外层都有两个未成对电子,L元素原子的基态未成对电子数是同周期最多的元素。
请回答如下问题:
(1)L元素在周期表中的位置是_______________,该原子核外电子排布式是_______________,其最高正价氧化物对应的水氧化物的化学式是_______________;
(2)元素X与Y形成的化合物晶体类型是晶体_________,1mol该化合物含有的化学键数为___________(用阿伏加德罗常数NA 表示);
(3)元素M是周期表中电负性最强的元素,X与M形成的化合物XM2的分子几何构型是________,该化合物中X的原子的杂化轨道类型是____________;
(4)X与碳、氢、三种元素形成的相对分子质量最小的分子里有个____δ键,____个π键;
(5)金属元素N与Z形成的离子化合物的晶胞结构如图,晶胞中Z离子数目为______。
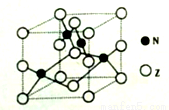
查看答案和解析>>
科目: 来源:2016届贵州市高三上学期第五次月考理综化学试卷(解析版) 题型:选择题
下列反应一定有沉淀生成的是:
A.将SO2通入BaCl2溶液中 B.将NH3通入AgNO3溶液中
C.将Cl2通入AgNO3溶液中 D.将NO2通入Ca(OH)2溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com