
科目: 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:选择题
下列有关实验操作、现象、解释和结论都正确的是( )
| 操 作 | 现 象 | 解释、结论 |
A | 过量的Fe粉中加入硝酸充分反应,滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
C | Al箔插入稀硝酸中 | 无现象 | Al在硝酸中钝化,形成致密的氧化膜 |
D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目: 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:选择题
根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4 ...... |
② | Cl2 、FeBr2 | FeCl3 、FeBr3 |
③ | MnO4- ...... | Cl2 、Mn2+ ...... |
A.第①组反应的其余产物为H2O和 O2
B.第②组反应中Cl2 与 FeBr2的物质的量之比为1︰1
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4- > Cl2 > Br2 > Fe3+
查看答案和解析>>
科目: 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.实验室存放HF的溶液,不能用带玻璃塞的细口瓶,而应用带橡胶塞的细口瓶。
B.碳酸氢镁溶液中加过量澄清石灰水的离子方程式为:
Ca2+ +Mg2++2OH- +2HCO3- =MgCO3↓+CaCO3↓+2H2O
C.水泥、玻璃和水晶都是硅酸盐产品
D.喝补铁剂时,加服维生素C,效果更好,原因是维生素C具有还原性
E.向新制的饱和氯水中分别加入CaCO3固体和Na2CO3固体,均会使得HClO的浓度增大
F.配制硫酸亚铁溶液时,为防止产生Fe3+,可在溶液中加入少量铁粉,为了抑制亚铁离子的水解,可在溶液中加入少量盐酸
G.无色溶液中,K+、Cl-、Na+、H2PO、PO、SO可以大量共存
H.由水电离的c(H+)=10-12mol/L的溶液中,ClO-、HCO、NO、NH、S2O可以大量共存
I.合金中一定有金属元素,两种不同的金属不一定可以加工成合金
J.某无色溶液含有下列离子中的若干种:H+、NH4+、Fe3+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。向该溶液中加入铝粉,只放出H2,则溶液中能大量存在的离子最多有5种
查看答案和解析>>
科目: 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:实验题
甲酸(HCOOH)是一种有刺激性气味的无色液体,有很强的腐蚀性。熔点8.4℃,沸点100.7℃,能与水、乙醇互溶,加热至160℃即分解成二氧化碳和氢气。
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH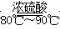 H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。
H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。
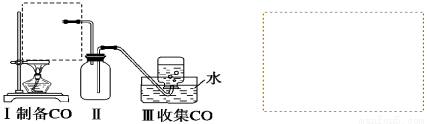
①从下图挑选所需的仪器,在虚线框中画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。
②装置Ⅱ的作用是_____________________________________________。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)2·4H2O]晶体。相关的化学方程式是:
2CuSO4+4NaHCO3===Cu(OH)2·CuCO3↓+3CO2↑+2Na2S O4+H2O
O4+H2O
Cu(OH)2·CuCO3+4HCOOH+5H2O===2Cu(HCOO)2·4H2O+CO2↑
实验步骤如下:
I.碱式碳酸铜的制备:

①步骤ⅰ是将一定量CuSO4·5H2O晶体和 NaHCO3固体一起放到研钵中研磨,其目的是___________。
NaHCO3固体一起放到研钵中研磨,其目的是___________。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃~80℃,如果看到______(填写实验现象),说明温度过高。
II.甲酸铜的制备:
将Cu(OH)2·CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的1/3时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
a、“趁热过滤”中,必须“趁热”的原因是 。
b、用乙醇洗涤晶体的目的是 。
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.1 mol Na2O2与SO2完全反应时转移电子数为NA
B.18g重水(D2O)所含的电子数为10NA
C.0. 5 mol NH4HSO4晶体中,含有H+数目约为0.5 NA
D.常温常压下,3gHCHO和CH3COOH的混合物中含有0.4NA个原子
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
离子方程式正确的是( )
A.0.01mol NH4Al(SO4)2溶液与0.01mol·L-1Ba(OH)2溶液等体积混合
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B.用惰性电极电解CuCl2溶液:2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
C.将标准状况下的11.2L氯气通入200mL2mol·L-1的FeBr2溶液中,离子反应方程式为:
4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl-
D.铁粉中滴加少量浓硝酸:Fe+3NO3-+6H+=Fe3++3NO2↑+3H2O
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图①所示,如果向所得的溶液中加入0.1molCu(OH)2后,使溶液恰好恢复到电解前的浓度和pH,电解过程中转移的电子为( )
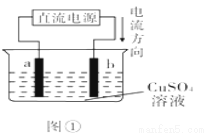
A. 0.2mol B. 0.4mol C. 0.6mol D. 0.8mol
查看答案和解析>>
科目: 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:实验题
在平板电视显示屏生产过程中产生的废玻璃粉末中含有二氧化铈(CeO2).
(1)在空气中煅烧Ce(OH)CO3可制备CeO2,该反应的化学方程式
(2)已知在一定条件下,电解熔融状态的CeO2可制备Ce,写出阴极的电极反应式 ;
(3)某课题组以上述废玻璃粉末(含有SiO2、Fe2O3、CeO2以及其他少量不溶于稀酸的物质)为原料,设计如图1流程对资源进行回收,得到Ce(OH)4和硫酸铁铵.

①得到滤渣B时,需要将其表面杂质洗涤干净.洗涤的操作是 .
②反应(1)的离子方程式为 .
③操作I的名称是
④如图2,氧化还原滴定法测定制得的Ce(OH)4产品的纯度.
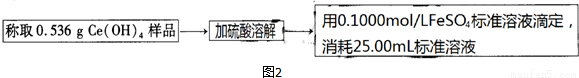
该产品中Ce(OH)4的质量分数为 (保留小数点后两位).若滴定所用FeSO4溶液已在空气中露置了一段时间,则测得该Ce(OH)4产品的纯度 (“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目: 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是( )
A、纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
B、煤经过气化和液化等物理变化可以转化为清洁燃料
C、侯氏制碱法的工艺过程中应 用了物质溶解
用了物质溶解 度的差异
度的差异
D、用硫酸清洗锅炉中的水垢
查看答案和解析>>
科目: 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:选择题
A的分子式为C8H16O2,可发生如下转化:
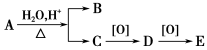
其中B与E互为同分异构体,则A可能的结构有( )
A.8种 B.4种 C.2种 D.1种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com