
科目: 来源:2016届内蒙古巴彦淖尔市高三上期中考试理化学试卷(解析版) 题型:填空题
将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品。回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾,溴,镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是:Br2+Na2CO3+H2O  NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为 mol。
NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为 mol。
(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:
离子 | Na+ | Mg2+ | Cl- | SO42- |
浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品2的化学式为 ,1L浓海水最多可得到产品2的质量为 g。
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 。
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:选择题
下列有关阿伏伽德罗常数NA说法错误的是
A.22 g 2H218O中含有的质子数为10NA
B.电解58.5 g熔融的NaCl,能产生11.2 L氯气(标准状况)、23.0 g金属钠
C.1.00 mol NaCl中,所有Na+的最外层电子总数为10NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:选择题
下列实验操作能达到目的的是
A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
B.制取二氧化氮时,用水或NaOH溶液吸收尾气
C.为测定Na2CO3和NaHCO3混合物中Na2CO3质量分数,取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b g,该方案可行。
D.为测定镀锌铁皮的锌层厚度,将镀锌铁皮与足量盐酸反应待气泡明显减少时取出,洗涤,烘干,称重。若烘干时间过长,会导致测定结果偏小。
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:选择题
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知

A.Y元素氧化物对应水化物的酸性一定弱于Z
B.W、X、Y中最简单氢化物稳定性最强的是X
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:实验题
毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2?2H2O的流程如下:
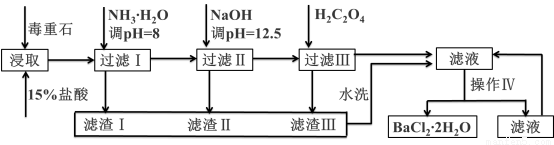
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀的pH | 11.9 | 9.1 | 1.9 |
完全沉淀的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)= 1.6×10–7,Ksp(CaC2O4)= 2.3×10–9
(1)实验室用37%的盐酸配制1mol/L盐酸,除烧杯外,还需要使用下列玻璃仪器中的:______________。
a.容量瓶 b.量筒 c.玻璃棒 d.滴定管
为了加快毒重石的酸浸速率,可以采取的措施有:_______________________。(至少两条)
(2)加入氨水调节溶液pH=8的目的是:________________________________。滤渣Ⅱ中含__________(填化学式)。加入H2C2O4时应避免过量,原因是:_____________________________。
(3)操作Ⅳ的步骤是:蒸发浓缩、冷却结晶、____________。
(4)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H2O Ba2++CrO42—=BaCrO4↓
步骤Ⅰ 移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
氯化钡溶液浓度为______________________ mol·L-1(用含字母的式子表示)。若步骤Ⅱ中滴加盐酸时有少量待测液溅出,则Ba2+浓度的测量值将___________(填“偏大”或“偏小”)。
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:实验题
ClO2与Cl2的氧化性相近,常温下均为气体,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)仪器C的名称是:___________。安装F中导管时,应选用图2中的:___________。(填“a”或“b”)
(2)打开B的活塞,A中氯酸钠和稀盐酸混和产生Cl2和ClO2,写出反应化学方程式:____;为使ClO2在D中被稳定剂充分吸收,可采取的措施是:__________________________。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是:_________________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:___________,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是:______________________ 。
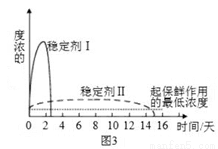
(5)已吸收ClO2气体的稳定剂Ⅰ和Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂的原因是 ________________。
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:填空题
扁桃酸衍生物是重要的医药中间体,以A和B 为原料合成扁桃酸衍生物F路线如下:

(1)A的分子式为C2H2O3,可发生银镜反应,且具有酸性,A所含官能团名称为:_______;写出A+B→C的化学反应方程式为__________________________。
(2)C中 ①、②、③3个—OH的酸性由强到弱的顺序是: _____________。
①、②、③3个—OH的酸性由强到弱的顺序是: _____________。
(3)E是由2分子C生成的含有3个六元环的化合物,E的分子中不同化学环境的氢原子有________种。
(4)D→F的反应类型是__________,1mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为:________mol。
写出符合下列条件的F的所有同分异构体(不考虑立体异构)的结构简式:_______________。
①属于一元酸类化合物;②苯环上只有2个取代基且处于对位,其中一个是羟基。
(5)写出D在稀NaOH溶液中的反应消耗NaOH的物质的量是____mol。
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:选择题
化学科学对提高人类生活质量和促进社会发展具有重要作用,下列说法正确的是
①汽车尾气的大量排放影响了空气的质量,但是不会造成PM2.5值升高
②研发安全特效药物,有利于人类抵御疾病
③规范食品添加剂的生产并科学使用,有利于保障人体健康和生命安全
④推广城市生活垃圾处理的减量化、资源化、无害化技术,有利于环境保护和资源充分利用
⑤用聚氯乙烯代替聚乙烯作食品包装袋,有利于节约使用成本
A.②③④ B.②④⑤ C.①③④ D.①②③
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:选择题
常温下,下列溶液中可能大量共存的离子组是
A.某中性溶液中: Na+、Fe3+、SO42-、NO3-
B.某无色溶液中: K+、Mg2+、ClO-、SO42- Fe2+
C.能使KSCN变红的溶液中: NH4+、Na+、SiO32-、HCO3-
D.水电离产生的c(OH-)=1×10-10mol/L的溶液中: Al3+、SO42-、NO3-、Cl-
查看答案和解析>>
科目: 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的相对位置如下所示,其中Z元素最外层电子数是其电子层数的2倍。下列说法正确的是
X | Y | |
Z | W |
A.四种短周期元素中W的原子半径最小
B.Z元素在周期表中的位置是第三周期第ⅣA族
C.原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z
D.元素非金属性由强到弱的顺序: W> Z,W的单质常温下可与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com