
科目: 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
常温下,将0.02 mol·L-1的Ba(OH)2溶液100 mL和0.02 mol·L-1的NaHSO4溶液100 mL混合,若忽略溶液体积变化,则混合后的溶液
A.pH=12
B.pH=2
C.由水电离产生的c(H+)=1.0×10-2 mol·L-1
D.溶质的物质的量浓度为0.02 mol·L-1
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
下列有关实验的做法正确的是
A.用pH试纸测氯水的pH
B.用托盘天平称取5.72 g NaCl晶体
C.用酸式滴定管量取20.00 mL的酸性KMnO4溶液
D.用带磨口玻璃塞的试剂瓶保存Na2CO3溶液
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:填空题
300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
(1)300℃时,该反应的平衡常数表达式为K=________已知K300℃<K350℃,则ΔH_______0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为___________,D的平均反应速率为___________。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:实验题
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察_________
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是___________________________
(5)如图,是某次滴定时的滴定管中的液面,其读数为 mL

(6)
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前度数(mL) | 滴定后度数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度 mol/L.
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上期中测试化学试卷(解析版) 题型:选择题
有甲乙两种烃,分子中碳的质量分数相同,则下列说法正确的是
A.甲和乙一定是同分异构体
B.甲和乙不可能是同系物
C.甲和乙各1mol完全燃烧后,生成的二氧化碳的质量一定相等
D.甲和乙的分子中,碳、氢原子个数之比相同
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上期中测试化学试卷(解析版) 题型:选择题
向pH相等的一元酸HA和HB溶液中分别加入适量的锌粒,充分反应后,当收集到的H2的体积相等时,消耗酸的体积V(HA)>V(HB),下列分析正确的是
A.消耗锌的质量:HA>HB B.HA一定为强酸
C.生成H2的平均速率:v(HA)< v(HB) D.酸性:HB>HA
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上期中测试化学试卷(解析版) 题型:选择题
为充分利用海洋资源,研究人员发明海水电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列说法错误的是
A.负极反应式: Ag+Cl-e-=AgCl
B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na2Mn5O10是还原产物
D.Cl-不断向电池的正极移动
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上期中测试化学试卷(解析版) 题型:填空题
(1)有下列五种烃:① 、②
、② 、 ③乙烷、④C(CH3)4、 ⑤
、 ③乙烷、④C(CH3)4、 ⑤ ,
,
其中互为同分异构体的是 (填序号),②与⑤之间的关系为 ,②③④⑤四种物质按它们的沸点由高到低的顺序排列正确的是 (填序号)。
(2)某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题:

写出A的电子式 ,E的结构简式为 。
(3)写出反应③的化学方程式,并注明反应类型:
,反应类型 。
(4)除去B中混有的少量杂质A,所用的试剂为 。
查看答案和解析>>
科目: 来源:2015-2016学年甘肃省高二上期中测试化学试卷(解析版) 题型:填空题
如图装置闭合电键K时,电流计A的指针将发生偏转。试回答:
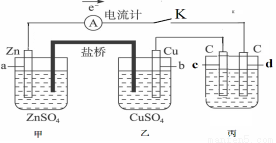
(1)若用此装置在铁制品上镀铜,在丙装置中,电极d应换成 。
(2)若丙池中的电解液为NaCl溶液,则电解时的离子方程式是 ;
(3)若丙池中的电解液为CuSO4溶液,则阳极的电极反应式为 ,电解时的化学反应方程式为 。
(4)若丙池中的电解液为500毫升1mol/L含CuSO4的NaCl溶液,当两极都生成11.2L(标况下)气体时,则丙池中CuSO4溶液的物质的量浓度是 。(忽略反应过程当中的体积变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com