
科目: 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:选择题
莫尔盐[(NH4)2Fe(SO4)2·8H2O]溶液经常用于定量滴定实验。下列有关说法正确的是
A.配制0.1mol•L-1莫尔盐溶液500mL,需莫尔盐19.6克
B.可与含Fe2+、HClO、H+、Cl-微粒的溶液大量共存
C.加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42-+Fe2++2OH-=2BaSO4↓+Fe(OH)2↓
D.取样,加入浓NaOH溶液并加热,出现可让蓝色石蕊试纸变红的气体,证明含NH4+
查看答案和解析>>
科目: 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:选择题
食品保鲜所用的“双吸剂”,是由还原剂、生石灰、氯化钠、炭粉等按一定比例组成的混合物,可吸收氧气和水。下列分析不正确的是( )
A.“双吸剂”中的生石灰有吸水作用
B.“双吸剂”吸收氧气时,发生了原电池反应
C.吸收氧气的过程中,铁作原电池的负极
D.炭粉上发生的反应为:O2+4e-+4H+=2H2O
查看答案和解析>>
科目: 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:推断题
A、B、C三种物质中均含有同一种元素,它们之间有如右图所示的转化关系(部分反应物质已略去)。
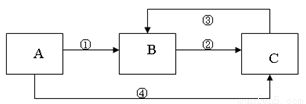
Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:______________,B溶液显酸性的原因(用离子方程式表示)_____________。
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是__________,A在氧气中燃烧产物所含的化学键有_______________;用C来制取B反应的化学方程式为______________________。
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式________________________。若只用一种试剂鉴别B、C,可以选的试剂是_____________。
查看答案和解析>>
科目: 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:实验题
氮化铝(AlN)是一种新型无机非金属材料,其制取原理为:
Al2O3+3C+N2 2AlN+3CO。在制取氮化铝时由于反应不完全,产品中有氧化铝和碳。
2AlN+3CO。在制取氮化铝时由于反应不完全,产品中有氧化铝和碳。
为了分析某AlN样品的组成,某实验小组进行了如下探究。
【实验1】测定样品中氮元素的质量分数。
取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).
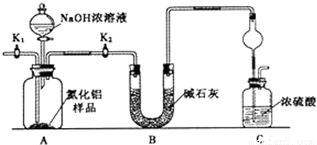
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(1)如图C装置中球形干燥管的作用是__________________________。
(2)完成以下实验步骤:组装好实验装置,首先___________,再加入实验药品.然后______,
打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,缓缓通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是__________。
(3)若去掉装置B,则导致测定结果____________(填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见_______________________。
【实验2】按以下步骤测定样品中铝元素的质量分数。
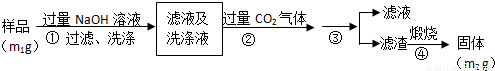
(4)步骤②生成沉淀的离子方程式为___________________。
(5)操作③需要的玻璃仪器有__________________________。
(6)A1元素的质量分数为________(用m1、m2表示)。
【实验3】测定样品中碳元素的质量分数。
称取10.00g样品置于反应器中,通往2.24LO2,在高温下充分反应后得到3.36L气体(AlN不跟O2反应),测得其密度为1.61g•L-1(体积及密度均已换算成标准状况)。
(7)计算该样品中碳元素的质量分数_____________。
查看答案和解析>>
科目: 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:选择题
在铁的氧化物和氧化铝组成的混合物中,加入2mol/L硫酸溶液65mL,恰好完全反应。所得溶液中Fe2+能被标准状况下112mL氯气氧化。则原混合物中金属元素和氧元素的原子个数之比为( )
A.5 : 7 B.4 : 3 C.3 : 4 D.9 : 13
查看答案和解析>>
科目: 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:选择题
能正确表示下列化学反应的离子方程式是 ( )
A.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
B.金属铝溶于盐酸中:Al+2H+=Al3++H2↑
C.硫化钠溶于水中:S2-+2H2O=H2S↑+2OH-
D.碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑
查看答案和解析>>
科目: 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:选择题
某无色混合气体可能由CH4、NH3、H2、CO、CO2和HCl中的某几种气体组成。在恒温恒压条件下,将此混合气体通过浓H2SO4时,总体积基本不变;通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使CuSO4粉末变色。则原混合气体的成份是
( )
A.HCl和CO B.HCl、H2和CO C.CH4和NH3 D.HCl、CO和CO2
查看答案和解析>>
科目: 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:实验题
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)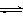 CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
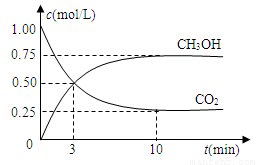
①从反应开始到平衡,氢气的平均反应速率v(H2)=___________mol/(L·min)。
②该反应的平衡常数表达式为__________________。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2 CO2=2 CO+O2,CO可用作燃料。
已知该反应的阳极反应为:4OH――4e―=O2↑+2H2O
则阴极反应式为:________________________________。
有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断是否可行并说出理由:__________________________________________。
查看答案和解析>>
科目: 来源:2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷(解析版) 题型:选择题
①钠比水轻;②钠的熔点较低;③钠与水反应时要放出热量;④钠与水反应后溶液呈碱性.某学生将一小块金属钠投入滴有酚酞试液的水中,该实验能证明上述四点性质中的
A.①④ B.①②④ C.①③④ D.①②③④
查看答案和解析>>
科目: 来源:2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷(解析版) 题型:选择题
水的相对分子质量为18,则一个水分子的质量为
A. B.
B. g·mol-1 C.18NA g D.
g·mol-1 C.18NA g D. g
g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com