
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
设NA代表,下列说法正确的是( )
常温常压下,氧气和臭氧的混合物16g中约含有NA个氧原子
B.标准状况下,11.2L H2O2中含分子数为0.5NA
C.标准状况下,22.4L H2中
D.100 mL 0.1 mol·L-1的FeCl3溶液中含有Fe3+的个数为0.01 NA
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
在水电离出的c(H+)=1×10-12 mol/L条件下,下列各组离子一定不能大量共存的是 ( )
A.NH4+、NO3-、Cl-、Na+ B.K+、SO32-、Cl-、NO3-
C.Na+、SO42-、Cl-、HCO3- D.Na+、NO3-、Fe3+、SO42-
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
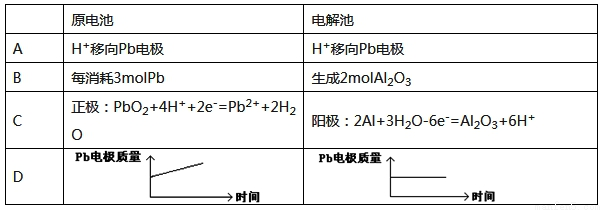
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O Al2O3+3H2↑ 电解过程中,以下判断正确的是( )
Al2O3+3H2↑ 电解过程中,以下判断正确的是( )
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应①Br2 + 2e- = 2Br-
②2Br- - 2e- = Br2 ③Zn – 2e- = Zn2+ ④Zn2+ + 2e- = Zn其中表示充电时的阳极反应和放电时的负极反应的分别是( )
A.②和③ B.②和① C.③和① D.④和①
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH  CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中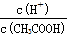 值增大,可以采取的措施是( )
值增大,可以采取的措施是( )
A.加少量烧碱溶液 B.降低温度 C.加少量冰醋酸 D.加水
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
100 mL 6 mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速度,但又不影响生成氢气的总量,不可向反应物中加入适量的( )
A.碳酸钠(固体) B.水
C.硫酸钾溶液 D.CH3COONa(固体)
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数Ksp(CaF2)=1.46×10-10 mol·L-3。现向1L 0.2 mol·L-1 HF溶液中加入1L 0.2 mol·L-1 CaCl2溶液,则下列说法中正确的是( )
A.25℃时,0.1 mol·L-1HF溶液中pH=1 B.KSP(CaF2)随温度和浓度的变化而变化
C.该体系中有CaF2沉淀产生 D.以上说法均不正确
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
已知:25℃时, Ksp[Mg(OH)2] = 5.61×10-12、Ksp [MgF2] =7.42×101。下列说法正确的是( )
A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者c(Mg2+)大
B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
C.25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1NH4Cl溶液中的Ksp小
D.25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成MgF2
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:填空题
(1)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)= mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1 mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是 mol·L-1。
(2)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至 。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至 。
(3)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液是 (填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= 。
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:填空题
在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16 g。试回答下列问题。
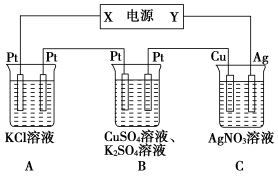
(1)电源中X电极为直流电源的________极。
(2)pH变化:A:________,B:________,C:________。(填“增大”、“减小”或“不变”)
(3)通电5 min时,B中共收集224 mL (标准状况下) 气体,溶液体积为200 mL,则通电前CuSO4溶液的物质的量浓度为________(假设电解前后溶液体积无变化)。
(4)若A中KCl足量且溶液的体积也是200 mL,电解后,溶液的pH为________(假设电解前后溶液体积无变化)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com