
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
在25℃时,有100g饱和Ca(OH)2溶液,向其中加入纯CaO粉末a g,反应后温度恢复到25℃,下列有关该溶液的说法正确的是
A.溶液中c(Ca2+)将增大 B.溶液的pH将增大
C.溶液中Ca2+总数将减少 D.溶液中c(OH-)减小
查看答案和解析>>
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
对于0.1mol•L-1 Na2CO3溶液,正确的是
A.升高温度,溶液的pH降低
B.c(Na+)=2c(CO32―)+c(HCO3―)+ c(H2CO3)
C.c(Na+)+c(H+)=2c(CO32―)+ 2c(HCO3―)+ c(OH―)
D.加入少量NaOH固体,c(CO32―)与c(Na+)均增大
查看答案和解析>>
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
可逆反应aA(s)+bB(g) cC(g) +dD(g), 当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是
cC(g) +dD(g), 当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是
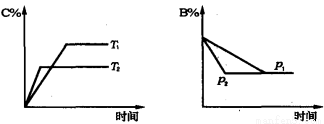
A.P1>P2,a+b=c+d
B.Pl<P2,b=c+d
C.T1>T2,正反应放热
D. Tl<T2,正反应吸热
查看答案和解析>>
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
反应SO2(g) + NO2(g)  NO(g) + SO3(g)在一定条件下建立平衡,保持温度和容器体积不变再加入一定量的O2,下列说法正确的是
NO(g) + SO3(g)在一定条件下建立平衡,保持温度和容器体积不变再加入一定量的O2,下列说法正确的是
A.平衡左移,容器内压强不一定增大
B.平衡右移,达到平衡时容器内压强一定增大
C.平衡右移,SO2的转化率提高
D.平衡不一定移动,容器内压强一定增大
查看答案和解析>>
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+ H2O(g) CO2 (g)+ H2(g)
CO2 (g)+ H2(g)
反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是
A.反应在t1min内的平均速率为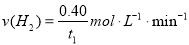
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时n(CO2)= 0.40mol
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时H2O转化率增大
D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
查看答案和解析>>
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:填空题
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ | 700 | 800 | 830 | 1000 | 1 |
平衡 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则 6s时c(A)= mol·L-1,C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ;
6s时c(A)= mol·L-1,C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ;
(3)1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡
A(g)+B(g)的平衡 常数的值为 。
常数的值为 。
查看答案和解析>>
科目: 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:填空题
已知:25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
Ba2+对人体有毒,医学上进行消化系统X射线透视时,常用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是:
__________________________________________________________。
万一误服了少量BaCO3,应尽快用大量0.5 mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为__________mol/L。
查看答案和解析>>
科目: 来源:2016届吉林省高三上第三次模拟考试理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.NaClO溶液中通入少量SO2:ClO-+SO2+H2O=2H++SO42-+Cl-
B.FeCl3溶液中通入过量H2S气体:2Fe3++3H2S=2FeS↓+S↓+6H+
C.Na2CO3溶液中通入少量Cl2:2CO32-+Cl2+H2O=ClO-+Cl-+2HCO3-
D.NaHSO3溶液中通入少量Cl2:HSO3-+Cl2+H2O=3H++SO42-+2Cl-
查看答案和解析>>
科目: 来源:2016届吉林省高三上第三次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.已知冰的熔化热为6.0 kJ﹒mol-1,冰中氢键键能为20 kJ﹒mol-1,假设1mol冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中30%的氢键
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,K a=(ca)2/C(1?a).若加入少量CH3COONa固体,则电离平衡CH3COOH CH3COO-+H+向左移动,a减小,Ka不变
CH3COO-+H+向左移动,a减小,Ka不变
C.检测得环已烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916kJ.mol-1、-3747 kJ.mol-1和-3265kJ.mol-1可以证明在苯分子中不存在独立的碳碳双键
D.进行中和热反应中,如果不把温度计上的酸用水冲洗掉,那么根据cm△t计算得到的Q结果会偏小
查看答案和解析>>
科目: 来源:2016届吉林省高三上第三次模拟考试理综化学试卷(解析版) 题型:填空题
AX(g)+2X2(g) AX5(g)在容积为10L恒定不变的密闭容器中进行。起始时AX和X2均为1.3mol,分三组进行实验,每组只改变一个条件且改变条件均不同。反应体系总压强随时间的变化如图所示。(计算结果均保留两位有效数字)
AX5(g)在容积为10L恒定不变的密闭容器中进行。起始时AX和X2均为1.3mol,分三组进行实验,每组只改变一个条件且改变条件均不同。反应体系总压强随时间的变化如图所示。(计算结果均保留两位有效数字)
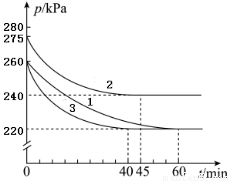
(1)计算实验1反应开始至达到平衡时的反应速率v(AX5)=________________。
(2)图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为______(填实验序号);
与实验1相比,其他两组改变的实验条件及判断依据是:2____________,3_________。
(3)用p1表示开始时总压强,p2表示平衡时总压强,α表示AX的平衡转化率,则α的表达式为____________;实验1和2的平衡转化率:α1为___________,α2为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com