
科目: 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:选择题
下列各组离子能在某无色溶液中大量共存的是
A.HSO3-、H+、MnO4-、K+ B.Cl-、NO3-、Fe2+、H+
C.Ba2+、OH-、Cl-、 Na+ D.NH4+、Na+、NO3-、OH-
Na+ D.NH4+、Na+、NO3-、OH-
查看答案和解析>>
科目: 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:选择题
下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的是
① NaHCO3 ②Na2CO3 ③NH4H CO3 ④SO2 ⑤ (NH4)2CO3
CO3 ④SO2 ⑤ (NH4)2CO3
A.①②③ B.②③④ C.①③⑤ D.全部
查看答案和解析>>
科目: 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:实验题
化学兴趣小组为了探究常温下某未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[ 提出猜想]
提出猜想]
猜想1:该气体为CO2。
猜想2: 。
猜想3:该气体为CO2和SO2的混合气体。
为了验证猜测,该小组设计实验加以探究:
[实验探究]
该小组同学按如图所示装置,将气体从a端通入,则:
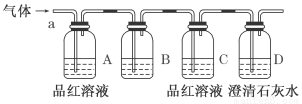
(1)B中应该装下列 试剂(填编号)。
A.NaOH溶液 B.酸性KMnO4溶液
C.盐酸 D.澄清石灰水
(2)B中溶液的作用是:  。
。
(3)D中澄清石灰水的作用是: 。
(4)通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
[得出结论]由上述现象该小组同学得出的结论为: 。
查看答案和解析>>
科目: 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:推断题
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
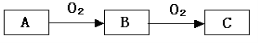
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 。将C长期露置于空气中,最后将变成物质D 。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能用下图装置制取的气体,请结合所学知识,回答下列问题:
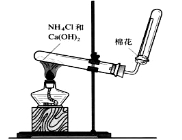
①写出实验室制取A的化学方程式 。
②收集A的方法是 ,验证A是否已经收集满的方法是:
(任 写一种)。
写一种)。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
查看答案和解析>>
科目: 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:选择题
下列说法中正确的是
A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) ΔH<0,则该反应一定能自发进行
B.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
C.催化剂可以加快化学反应速率,也能增大化学反应的焓变
D.NH3·H2O溶液加水稀释后,溶液中的pH值增大
查看答案和解析>>
科目: 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:选择题
下列图示与对应的叙述不相符的是
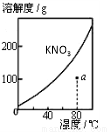



图1 图2 图3 图4
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1醋酸溶液得到的滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目: 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:选择题
某同学按如下图所示的装置进行实验。A、B为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析正确的是
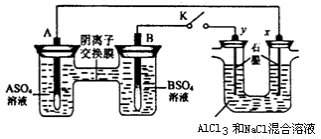
A.溶液中c(A2+)减小
B.B的电极反应:B-2e- =B2+
C.y电极上有H2产生,发生还原反应
D.反应初期,x电极周围出现白色胶状沉淀,一段时间以后沉淀逐渐溶解
查看答案和解析>>
科目: 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:选择题
现有0.4 mol·L-1HA溶液和0.2 mol·L-1NaOH溶液等体积混合组成的混合溶液。下列有关推断正确的是
A.若该溶液中HA的电离能力大于A-的水解能力,则有c(Na+)>c(A-)> c(HA)> c(H+)>c(OH-)
B.若该溶液中A-的水解能力大于HA的电离能力,则有c(A-)>c(HA)>c(Na+)> c(OH-)>c(H+)
C.无论该溶液呈酸性还是碱性,都有c(Na+)+c(H+)=c(A-)+c(OH-)
D.无论该溶液呈酸性还是碱性,都有c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目: 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:填空题
汽车尾气中的主要污染物是NO和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)已知:2NO(g)+2CO(g) 2CO2(g)+N2(g) △H=-746.5KJ/mol(条件为使用催化剂)
2CO2(g)+N2(g) △H=-746.5KJ/mol(条件为使用催化剂)
2C (s)+O2(g) 2CO(g) △H=-221.0KJ/mol
2CO(g) △H=-221.0KJ/mol
C (s)+O2(g) CO2(g) △H=-393.5KJ/mol
CO2(g) △H=-393.5KJ/mol
则N2(g)+O2(g)=2NO(g) △H= kJ·mol-1。
(2)T℃下,在一容积不变的密闭容器中,通入一定 量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
C(NO)10- | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
C(CO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
则c1合理的数值为 (填字母标号)。
A.4.20 B.4.00 C.3.50 D.2.50
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率。根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如下图所示:
实验 编号 | T/°C | NO初始浓 度/10-3mol•L-1 | CO初始浓 度/10-3mol•L-1 | 催化剂的比 表面积/m2•g-1 |
① | 350 | 1.20 | 5.80 | 124 |
② | 280 | 1.20 | 5.80 | 124 |
③ | 280 | 1.20 | 5.80 | 82 |

则曲线I对应的实验编号为 。
(4)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
H2O | CO | CO | H2 | |||
① | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
② | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
③ | 900 | a | b | c | d | t |
①实验组①中以v(CO2)表示的反应速率为 。
②若a=2,b=1,则c= ,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系为:α2 (H2O) α3 (CO)(填“<”、“>”或“=”)。
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。
①则负极的电极反应式为______________ __。
__。

② 以上述电池为电源,通过导线连接成图一。若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式 。电解一段时间后,取25mL上述电
以上述电池为电源,通过导线连接成图一。若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式 。电解一段时间后,取25mL上述电 解后的溶液,滴加0.4mol/L醋酸得到图二曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。根据图二计算,上述电解过程中消耗一氧化碳的质量为__________g。
解后的溶液,滴加0.4mol/L醋酸得到图二曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。根据图二计算,上述电解过程中消耗一氧化碳的质量为__________g。
查看答案和解析>>
科目: 来源:2015-2016学年湖南二校高一理科实验班上联考2化学卷(解析版) 题型:选择题
下列各组中两种气体所含的原子数一定相等的是( )
A.温度相同,体积相同的O2和N2
B.质量相等,密度不等的N2和CO
C.体积相等,密度相等的CO和C2H4
D.压强相同、体积相同的N2和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com