
科目: 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.乙醇既可以发生催化氧化反应,又可以发生酯化反应
B.用溴水可以鉴别乙醇、乙酸和苯
C.糖类、油脂、蛋白质三类物质都只含有C、H、O三种元素
D.C5H10O属于醛类的同分异构体为六种
查看答案和解析>>
科目: 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列判断正确的是:
A.原子半径:S>O>N B.沸点:H2O>HF>H2S
C.离子半径:Cl->Al3+>Mg2+ D.还原性:I->S2->Br-
查看答案和解析>>
科目: 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
关于下列图示的说法中正确的是:
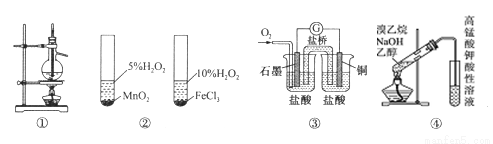
A.图①装置用于分离沸点相关较大的互溶液体混合物
B.图②装置用于研究不同催化剂对反应速率的影响
C.图③中电流计的指针发生偏转,石墨为正极
D.图④装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯
查看答案和解析>>
科目: 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是:
A.某HCl溶液的pH值为2,则溶液中由水电离的c(H+)=10-2mol•L-1
B.0.1 mol•L-1的KHA溶液,其pH=10, c(K+)>c(A2-)>c(HA-)>c(OH-)
C.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D.将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后溶液pH>7,则反应后的混合液:c(HA)>C(Na+)>c(A-)
查看答案和解析>>
科目: 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
一定条件下合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是:
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是:
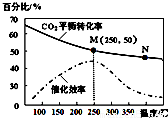
A.生成乙烯的速率:v(M)有可能小于v(N)
B.平衡常数:KM>KN
C.当温度高于250℃,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低
D.若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7%
查看答案和解析>>
科目: 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:推断题
A、B、D、R、Q五种短周期主族元素,其原子序数依次增大,其中A原子核内无中子,B与D同周期,R与Q同周期,A与R同主族,D与Q同主族,D元素的原子最外层电子数是次外层电子数的三倍,B元素的最高正价和最低负价代数和为2。请用对应的化学用语回答下列问题:
(1)Q元素位于元素周期表中第______周期_____族。
(2)D、R、Q三种元素形成的简单离子的半径由大到小的顺序是________(用离子符号表示)。
(3)由A、B两种元素以原子个数比为5:1形成的离子化合物X,X的电子式为_______。
(4)由A、B元素形成的A2B4可以与O2、KOH溶液形成原电池,该原电池负极的电极反应式为____。
(5)由A、D、R、Q四种元素形成的化合物Y(RAQD3)(已知A2QD3的Ka1=1.2×10-2、Ka2=6.3×10-8),则Y溶液中各离子浓度由大到小的顺序为_______________;室温下,向Y溶液中加入一定量的NaOH,使溶液中c(AQD3-)=c(QD32-),则此时溶液呈______(填“酸性”、“碱性”或“中性”)
(6)Fe与D元素可形成Fe2D3、Fe3D4等化合物。向5.2g Fe2D3、Fe3D4、Cu的混合中加入0.5mol/L的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为______g。
查看答案和解析>>
科目: 来源:2016届云南师范大学附属中学高三上高考适应性月考化学试卷(解析版) 题型:选择题
化学用语是学习化学的工具和基础。下列有关化学用语的表达正确的是
A.质量数为37的氯原子:1737Cl
B.Al(OH)3的电离方程式:H++AlO2-+H2O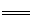 Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-
C.CO2的结构式:O=C=O
D.次氯酸分子的电子式: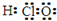
查看答案和解析>>
科目: 来源:2016届云南师范大学附属中学高三上高考适应性月考化学试卷(解析版) 题型:选择题
下列关于有机物的说法正确的是
A.乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色
B.CH CH和CH2=CHCH=CH2互为同系物
CH和CH2=CHCH=CH2互为同系物
C.乙酸乙酯在碱性条件下的水解反应皂化反应
D.2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同
查看答案和解析>>
科目: 来源:2016届云南师范大学附属中学高三上高考适应性月考化学试卷(解析版) 题型:填空题
铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)工业上,向炽热铁屑中通入氯化氢可生成无水氯化亚铁,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是____________________;为防止FeCl2溶液中含有FeCl3,最好在FeCl2溶液中加入___________。
(2)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,同时伴随产生一种可燃性气体,该反应的化学方程式为___________。
若有1molC参与反应,则转移的电子数目为___________。
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开,只允许锂离子通过)工作原理为FePO4+Li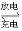 LiFePO4,如下图所示。则放电时FePO4一端为电池的_____极,充电时阳极上的电极反应式为__________________。
LiFePO4,如下图所示。则放电时FePO4一端为电池的_____极,充电时阳极上的电极反应式为__________________。
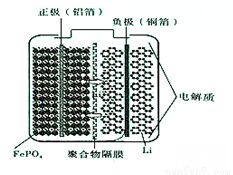
(3)硫化亚铁常用于工业废水的处理。已知:25℃时,溶度积常数Ksp(FeS)=6.3×10-18、Ksp(CdS)=3.6×10-29.请写出用硫化亚铁处理含Cd2+的工业废水的离子方程式__________________,在FeS、CdS的悬浊液中c(Fe2+):c(Cd2+)=______________。
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5mol/L 100mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入___________ml、2mol/L的盐酸(忽略加入盐酸体积)。
查看答案和解析>>
科目: 来源:2016届云南师范大学附属中学高三上高考适应性月考化学试卷(解析版) 题型:填空题
[化学—选修2:化学与技术]
煤炭被人们誉为黑色的“金子”,它是人类使用的主要能源之一。为了提高煤的利用率,减少有害气体的排放,人们采取了各式各样的方法。
(1)煤的气化和液化可能提高煤的利用率。煤的气化技术的主要产物是___________。煤的液化技术又分为直接液化和间接氧化.将煤隔绝空气加强热得到焦炉气、煤焦油及焦炭等产品的技术称为___________。
(2)煤在燃烧前、后及燃烧过程中均可采取措施减少有害气体的排放.
①在燃烧前,可以采用微生物脱硫技术.原理如下:

上述过程中Fe2+的作用为________________。写出Fe2+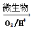 Fe3+的离子方程式________________。
Fe3+的离子方程式________________。
②煤在燃烧时,进行脱硫处理,常采用________燃烧技术,在把煤和脱硫剂加入锅炉燃烧室,使煤与空气在流化过程中充分混合、燃烧,起到固硫作用.常用脱硫剂的主要化学成分为_______(填化学式)。
③煤在燃烧后,烟气净化常采用除尘技术和脱硫、脱硝技术.湿法脱硫、脱硝技术中将烟气通入_________设备,用石灰水淋洗。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com