
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
有一处于平衡状态的反应:X(g)+3Y(g) 2Z(g) △H<0,为了使平衡向生成Z的方向移动,应选择的条件是
2Z(g) △H<0,为了使平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤ B.②③⑤ C.②④⑥ D.②③⑥
查看答案和解析>>
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
某反应的△H=+100kJ/mol,下列有关该反应的叙述正确的是
A.正反应活化能小于100kJ•mol-1
B.正反应活化能不小于100kJ•mol-1
C.正反应活化能比逆反应活化能大100kJ•mol-1
D.逆反应活化能一定小于100kJ•mol-1
查看答案和解析>>
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
已知反应:①2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol 下列结论正确的是
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量
D.稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol
查看答案和解析>>
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
对于可逆反应H2(g)+I2(g) 2HI(g),在一定温度下由H2(g)和I2(g)开始反应,下列说法正确的是
2HI(g),在一定温度下由H2(g)和I2(g)开始反应,下列说法正确的是
A.H2(g)的消耗速率与HI(g)的生成速率之比为2:1
B.正、逆反应速率的比值是恒定的
C.反应进行的净速率是正、逆反应速率之差
D.达到平衡时,正、逆反应速率相等
查看答案和解析>>
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
反应N2O4(g) 2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
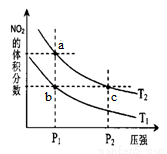
A.a、c两点的反应速率:a>c
B.a、c两点气体的颜色:a浅,c深
C.a、b两点气体的平均相对分子质量:a>b
D. b、c两点化学平衡常数:b<c
查看答案和解析>>
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:填空题
汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物:CmHn(烃)、SO2、NOx、CO和C等,请回答下列有关问题:
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为________________,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由________能转化为________能,最终转化为机械能;
(2)通过车用燃油的精炼加工处理,可减少汽车尾气中的__________(填化学式,多填本空不得分)排放;
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOX与CO反应的化学方程式________。
查看答案和解析>>
科目: 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:填空题
煤气化和液化是现代能源工业中重点考虑的能量综合利用方案。最常见的气化方法为用煤生成水煤气,而当前比较流行的液化方法用煤生成CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1
2CO(g)+O2(g)=2CO2(g) △H2
2H2(g)+O2(g)=2H2O(g) △H3
则反应CO(g) +2H2(g)=CH3OH(g) 的△H=_______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
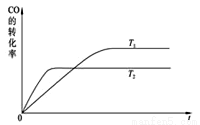
①T1和T2温度下平衡常数大小关系是K1____K2(填“>”“<”或“=”)。
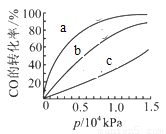
②由CO合成甲醇时,CO在250℃、300℃、350℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为______℃,实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是______。
③以下有关该反应的说法正确的是_________(填序号)。
A.恒温、恒容条件下同,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2molCO和6molH2充入2L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为80%
(3)一定温度下,向2L固定体积的密闭容器中加入1molCH3OH,发生反应:CH3OH(g)  CO(g) +2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g) +2H2(g),H2的物质的量随时间变化的曲线如图所示。
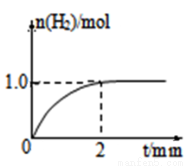
0~2min内的平均反应速率v(CH3OH)= ____________;该温度下,CO(g)+2H2(g) CH3OH(g)的平衡常数K=____________;相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_____ 是原来的2倍.
CH3OH(g)的平衡常数K=____________;相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_____ 是原来的2倍.
A.平衡常数 B.CH3OH的平衡浓度 C.达到平衡的时间 D.平衡时气体的密度
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
将下列各组物质按酸、碱、盐分类依次排列,正确的是
A.硫酸、纯碱、小苏打 B.磷酸、熟石灰、苛性钠
C.硫酸氢钠、生石灰、醋酸钠 D.硫酸、烧碱、胆矾
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
pH=1的无色透明溶液中,能大量共存的离子组是
A.Al3+、Ag+、HCO3-、Cl- B.Mg2+、NH4+、NO3-、Cl-
C.Ba2+、K+、Fe3+、Cl- D.K+、Na+、OH-、CO32-
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法中正确的是
A.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
B.1mol CO2和NO2的混合物中含的氧原子数为4NA
C.标准状况下,NA个CCl4分子所占的体积约为22.4L
D.54g H2O中含有3NA个水分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com