
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
在半导体生产或灭火剂的使用中,会向空气逸出气体如:NF3、CHClFCF3、C3F8,它们虽是微量的,有些确是强温室气体。下列推测不正确的是 ( )
A.由价层电子对互斥理论可确定NF3分子呈三角锥型
B.C3F8在CCl4中的溶解度比水中大
C.CHClFCF3存在手性异构
D.第一电离能:N<O<F
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
某晶体中含有极性键,关于该晶体的说法错误的是( )
A.不可能有很高的熔沸点 B.不可能是金属晶体
C.可能是有机物 D.可能是离子晶体
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
关于晶体的叙述中,正确的是 ( )
A.原子晶体中,共价键的键能越大,熔、沸点越高
B.分子晶体中,分子间的作用力越大,该分子越稳定
C.分子晶体中,共价键的键能越大,熔、沸点越高
D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
下列各组物质中,按熔点由低到高的顺序排列正确的是( )
①Na、K、Rb ②CO、KCl、SiO2 ③O2、I2、Hg ④Na、Mg、Al
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
右图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价,则Q的化合价为( )

A. -2 B. +2 C. +3 D. -3
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.由于铵盐是由离子键构成的,因而化学性质相当稳定
B.分子晶体中都存在分子间作用力,但可能不存在共价键
C.在常见的四种晶体类型中,都有“原子(离子)半径越大,物质熔点越低”的规律
D.常温下为气态或液态的物质,其固态时一定会形成分子晶体
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
有一种蓝色晶体[可表示为:MxFey(CN)6],经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如图所示。下列说法正确的是 ( )。
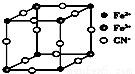
A.该晶体属于分子晶体,化学式为MFe2(CN)6
B.该晶体属于离子晶体,M呈+1价
C.该晶体属于离子晶体,M呈+2价
D.晶体中与每个Fe3+距离最近且等距离的CN-为12个
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:填空题
过渡元素在生活、生产和科技等方面有广泛的用途。
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色,据此判断,[Mn(H2O)6]2+________(填“有”或“无”)颜色。
(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是________。(填序号)
A.PFS中铁显+3价
B.铁原子的外围电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
元素 | Mn | Fe | |
电离能 | I1 | 717 | 759 |
(kJ·mol-1)[ | I2 | 1 509 | 1 561 |
I3 | 3 248 | 2 957 | |
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬(Ⅲ)与甲基丙烯酸根的配合物为: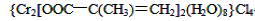
①该化合物中存在的化学键类型有______________________________。
②甲基丙烯酸分子中C原子的杂化方式有________。
③等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是________(填一种即可)。
④与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是________(填元素符号)。
查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:填空题
用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为________;Cu的原子半径为________cm(阿伏加德罗常数为NA,列出计算表达式,不用化简)。

查看答案和解析>>
科目: 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:推断题
已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素。其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外价电子数与B相同,其余各层均充满。B、E两元素组成化合物B2E的晶体为离子晶体。C、F的原子均有三个能层,C原子的第一至第四电离能(KJ·mol-1)分别为578、1 817、2 745、11 575;C与F能形成原子数目比为1∶3、熔点为190 ℃的化合物Q。
(1)B的单质晶体为体心立方堆积模型,其配位数为____________;E元素的最高价氧化物分子的立体构型是________________。F元素原子的核外电子排布式是_______________,G的高价离子与A的简单氢化物形成的配离子的化学式为________________。
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由________________。
(3)A、G形成某种化合物的晶胞结构如图所示。若阿伏加德罗常数为NA,该化合物晶体的密度为a g·cm-3,其晶胞的边长为________ cm。
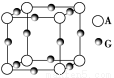
(4)在1.01×105 Pa、T1 ℃时,气体摩尔体积为53.4 L·mol-1,实验测得Q的气态密度为5.00 g·L-1,则此时Q的组成为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com