
科目: 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:选择题
下列物质分类正确的是
① 混合物:铝热剂、福尔马林、水玻璃、漂白粉 ② 化合物:CaCl2、烧碱、聚乙烯、HD
③ 电解质:明矾、绿矾、冰醋酸、硫酸钡 ④ 同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑤ 同素异形体:C60、C70、金刚石、石墨
A. ①②④ B.②③④ C. ①③⑤ D .②④⑤
查看答案和解析>>
科目: 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:选择题
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是
A.SiH4的沸点高于CH4,可推测PH3的沸点高于NH3
B.根据主族元素最高正化合价与族序数的关系,推出氧族元素最高正价都是+6
C.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO
D.根据HCl的酸性远强于H2S,可推出结合质子能力:S2-<Cl-
查看答案和解析>>
科目: 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:选择题
氮化铝(AlN)是一种新型无机材料,广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C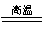 2AlN+3CO合成。已知AlN可与NaOH溶液反应放出有刺激性气味的气体。下列叙述正确的是
2AlN+3CO合成。已知AlN可与NaOH溶液反应放出有刺激性气味的气体。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1molAlN需转移6mol电子
C.AlN属于离子化合物,其中氮元素的化合价为+3
D.AlN与NaOH溶液反应的化学方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑
查看答案和解析>>
科目: 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:填空题
W、X、Y和Z都是周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④X的最外层电子数是其电子层数的2倍;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)Z元素在元素周期表中的位置为_________,化合物WY的电子式为_______________________________。
(2)实验室用 WX2与饱和食盐水来制某种气态有机化合物,反应的化学方程式为
___________________________________________________________________________。
(3)Cu2Z与过量浓硝酸反应有红棕色气体生成,反应的离子方程式为
______________________________________________________________________________。
查看答案和解析>>
科目: 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:实验题
酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:
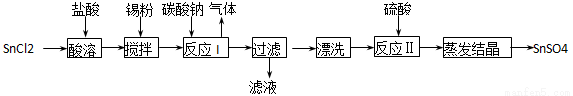
回答下列问题:
(1) SnCl2用盐酸而不用水直接溶解的原因是:_______________;加入锡粉的作用是:_______________;
(2) 反应I生成的沉淀为SnO,写出该反应的化学方程式:_______________;
(3) 检验沉淀已经“洗涤”干净的操作是:______________________________;
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH。若溶液中c(Sn2+)=1.0mol·L-1,则室温下应控制溶液pH _______________。(已知:Ksp[Sn (OH)2]=1.0×10-26)
(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:_______________。
查看答案和解析>>
科目: 来源:2016届湖南师范大学附属中学高三上月考(四)化学试卷(解析版) 题型:选择题
下列关于有机物的叙述不正确的是
A.C4H8O2的酯有4种结构
B.淀粉和纤维素互为同分异构体
C.乙醇和葡萄糖均能发生酯化反应
D.漂粉精和医用酒精均可用作消毒剂
查看答案和解析>>
科目: 来源:2016届湖南师范大学附属中学高三上月考(四)化学试卷(解析版) 题型:选择题
下列应用不涉及氧化还原反应的是
A.铝热法冶炼难熔金属
B.工业上电解熔融状态Al2O3制备Al
C.Na2O2用作呼吸面具的供氧剂
D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
科目: 来源:2016届湖南师范大学附属中学高三上月考(四)化学试卷(解析版) 题型:选择题
下列推测或结论不合理的是
A.X2-和Y+核外电子层结构相同,原子序数:X<Y
B.气态氢化物的稳定性HCl> HBr,还原性:Cl- >Br一
C.硅、锗都位于金属与非金属的交界处,用途:都可以做半导体材料
D.铷(37Rb)和锶(38Sr)分别位于第五周期lA和ll A族,碱性:RbOH>Sr(OH)2
查看答案和解析>>
科目: 来源:2016届湖南师范大学附属中学高三上月考(四)化学试卷(解析版) 题型:选择题
球墨铸铁中含有一种铁碳化合物X。实验室测定化台物X的组成实验如下:

下列说法不正确的是
A.固体2是Fe2O3
B.溶液甲中可能含有Fe3+
C.X的化学式可以表示为Fe3C2
D.X与足量的热浓硝酸反应有NO2和CO2生成
查看答案和解析>>
科目: 来源:2016届湖南师范大学附属中学高三上月考(四)化学试卷(解析版) 题型:实验题
SO2是常见的大气污染物,燃煤是产生SO2的主要原因。工业上有多种方法可以减少SO2的排放。
(1)往煤中添加一些石灰石,可使燃煤过程中产生的SO2转化成硫酸钙。该反应的总化学方程式是___________________________________。
(2)可用多种溶液做燃煤烟气中SO2的吸收液。
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHS03时,两种吸收液体积比V(Na2SO3): V(NaOH)= 。
②NaOH溶液吸收了足量的:SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式是 。
(3)甲同学认为BaCl2溶液可以做SO2的吸收液。为此甲同学设计如下实验(夹持装置和加热装置略,气密性已检验)。反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B中有白色沉淀。甲同学认为B中白色沉淀是SO2与BaCl2溶液反应生成的BaSO3,所以BaCl2溶液可做SO2 吸收液。
吸收液。
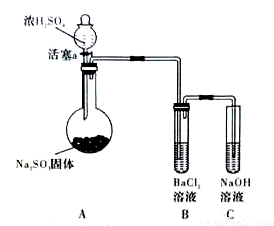
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是:
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCI2溶液反应生成BaSO4沉淀。
② 。
为证明 SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略,气密性已检验):
SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略,气密性已检验):
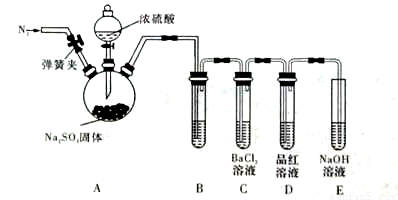
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其它现 象;D中红色褪去。
象;D中红色褪去。
③试管B中试剂是 溶液;滴加浓硫酸之前的操作是 。
④通过甲、乙两位同学的实验,得出的结论是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com