
科目: 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:选择题
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)  2CO2(g)+S(l) △H < 0,若反应在恒容的密闭容器中进行,下列有关说法不正确的是
2CO2(g)+S(l) △H < 0,若反应在恒容的密闭容器中进行,下列有关说法不正确的是
A.其它条件不变,使用不同催化剂,该反应的平衡常数不变
B.平衡前,随着反应的进行,容器内压强始终不变
C.平衡时,其它条件不变,分离出少量的硫,正反应速率不变
D.平衡时,其他条件不变,升高温度可使反应速率加快,平衡常数减小
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:选择题
在3个2 L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)  2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下: 
下列说法不正确的是( )
A.容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol·L-1·min-1
B.2c1<1.5
C.在该温度下甲容器中反应的平衡常数K=
D.2ρ1=ρ2
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:实验题
《化学反应原理》一书中,我们学习了两个重要的定量实验。请回答下列问题:
I.某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol·L-1 盐酸、0.55mol·L-1 NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
实 验 试剂如下 | 溶 液 温 度 | 中和热 △H | ||||
t1 | t2 | |||||
① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | ||
② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | ||
已知:Q(放)=C m(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1·Kg-1,m指溶液的质量,各物质的密度均为1g·cm-3。
①计算分析△H= 。(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
II.为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10 mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为
(2) 完成并配平下列离子方程式
C2O42- + MnO4- + H+ = CO2 + Mn2+ +
(3) 步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数 。(填“偏大”、“偏小”或“无影响”)
(4) 步骤③中判断滴定终点的方法是 。
(5)常温下0.01 mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示

①写出H2C2O4的电离方程式_________ __________________。
②KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题) _______________
③向0.1 mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是______。
A.c K+) = c(HC2O4-) + c(H2C2O4) + c(C2O42-)
B.c(Na+) = c(H2C2O4) + c(C2O42-)
C.c(K+) + c(Na+) = c(HC2O4-) + c(C2O42-)
D.c(K+) > c(Na+)
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二上期中考试化学试卷(解析版) 题型:选择题
下列有关热化学方程式的叙述正确的是( )
A.I2(g)+ H2(g)=2HI(g) △H1;I2(s)+ H2(g)=2HI(g) △H2,则△H1>△H2
B.2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ·mol-1,则氢气燃烧热为285.8kJ·mol-1
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.65kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq)=CH3COONa(aq) + H2O(l) △H =-57.3kJ·mol-1
D.已知2SO2(g)+O2(g) 2SO3 (g);△H=-QkJ·mol-1(Q>0),则将16gSO2(g)和足量O2置于一密闭容器中,充分反应后放出0.25QkJ的热量
2SO3 (g);△H=-QkJ·mol-1(Q>0),则将16gSO2(g)和足量O2置于一密闭容器中,充分反应后放出0.25QkJ的热量
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二上期中考试化学试卷(解析版) 题型:选择题
对可逆反应2A(s)+3B(g)  C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二上期中考试化学试卷(解析版) 题型:简答题
按要求回答下列问题:
(1)有下列六种物质:①碳60(C60)晶体②硼晶体③Na2O晶体④ CaF2晶体⑤P4O10晶体⑥碳化硅晶体。其中属于离子晶体的是 ,属于分子晶体的是 ,属于原子晶体的是________________。
(2)有下列分子:HCN、P4、SO2、PCl3、BF3,其中属于非极性分子的是 。
(3)有下列离子:SO32-、SO42-、CO32-,其中空间构型为正四面体形的是 ,中心原子的杂化轨道类型属于sp2杂化的是 。
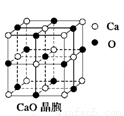
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为___________;与每一个钙离子距离最近并且距离相等的钙离子有____________个 。
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
下列关于能量转换的认识中不正确的是
A.电解水生成氢气和氧气时,电能转化成化学能
B.煤燃烧时化学能主要转变成热能
C.绿色植物光合作用过程中太阳能转变成化学能
D.白炽灯工作时电能全部转变成光能
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.李比希燃烧法、钠熔法、铜丝燃烧法都是用来分析有机物元素组成的方法
B.红外光谱法、紫外光谱法、核磁共振、质谱仪等都是现代化学测定有机物结构的常用方法
C.同位素示踪法是研究化学反应历程的手段之一
D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
水中加入下列溶液对水的电离平衡不产生影响的是
A.NaHSO4溶液 B. NaCl溶液 C.KAl(SO4)2溶液 D. KF 溶液
查看答案和解析>>
科目: 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某溶液中由水电离出来的氢离子浓度c(H+)=1×10-14 mol·L-1,在这种溶液里可能大量共存的离子组是
A.Al3+、NH4+、SO42-、Cl-
B.K+、Fe2+、MnO4-、Cl-
C.NH4+、SiO32-、NO3-、K+
D.Na+、K+、HCO3-、Mg2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com