
科目: 来源:专项题 题型:填空题
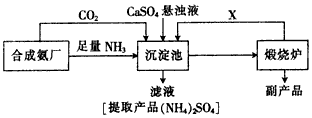
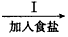 A和食盐的饱和溶液
A和食盐的饱和溶液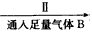 悬浊液
悬浊液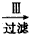 晶体
晶体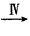 纯碱
纯碱
查看答案和解析>>
科目: 来源:北京期末题 题型:填空题
查看答案和解析>>
科目: 来源:0116 期末题 题型:单选题
查看答案和解析>>
科目: 来源:0116 期末题 题型:单选题
查看答案和解析>>
科目: 来源:0103 期末题 题型:单选题
查看答案和解析>>
科目: 来源:0118 期末题 题型:单选题
查看答案和解析>>
科目: 来源:模拟题 题型:单选题
查看答案和解析>>
科目: 来源:江苏模拟题 题型:填空题
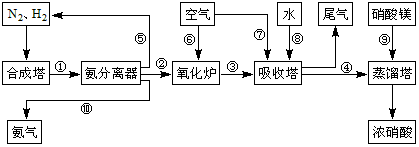
 CO2+H2
CO2+H2 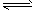 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中 T1____573K(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中 T1____573K(填“>”、“<”或“=”)。 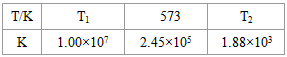
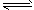 4NO(g)+6H2O(g) △H=
4NO(g)+6H2O(g) △H=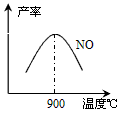
查看答案和解析>>
科目: 来源:0110 期末题 题型:单选题
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
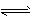 2NH3 ( g) △H = -a kJ . mol-1
2NH3 ( g) △H = -a kJ . mol-1 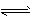 NH3(g) △H = -b kJ . mol-1
NH3(g) △H = -b kJ . mol-1 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com