
科目: 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列叙述的事实与盐类水解无关的是( )
A.金属焊接时可用NH4Cl溶液作除锈剂
B.配制FeSO4溶液时,加入一定量Fe粉
C.长期施用铵态氮肥会使土壤酸化
D.向FeCl3溶液中加入CaCO3粉末后有气泡产生
查看答案和解析>>
科目: 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:选择题
常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中正确的是(忽略混合前后溶液体积变化)( )
A.溶液的pH值:①>③>②
B.水电离出的c(OH-):③>①=②
C.①和③等体积混合后的溶液:c(CH3COOH)+c(CH3COO-)=0.1mol/L
D.②和③等体积混合后的溶液:c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
科目: 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:填空题
某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处) KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作为:
A.将碘的四氯化碳溶液置于分液漏斗中;
B.加入适量Na2SO3稀溶液;
C.分离出下层液体;
D.将分液漏斗充分振荡后静置
其中分液漏斗使用前须进行的操作是 ,上述操作正确的顺序是: (填序号)
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
A.准确称取wg食盐,加适量蒸馏水使其完全溶解;
B.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
C.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示) mg/kg。
查看答案和解析>>
科目: 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:填空题
电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25 ℃):
化学式 | 电离平衡常数 |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1)25 ℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为________________________________。(填写序号)
(2)25 ℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为______ ___。
(3)现有浓度为0.02 mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是 。
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN) = c(OH-)
D.c(HCN)+ c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理_____________________。
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小___________________;电荷守恒表达式 ___________________ 。
(6)H2C2O4溶液和KMnO4酸性溶液可发生反应:H2C2O4+MnO4-+H+→CO2+Mn2++H2O,反应中每生成标况下4.48LCO2气体,外电路中通过的电子的物质的量为__________mol。
查看答案和解析>>
科目: 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法错误的是
A.已知N2(g)+3H2(g) 2NH3(g) △H=﹣92.4kJ•mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ•mol﹣1
2NH3(g) △H=﹣92.4kJ•mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ•mol﹣1
B.1mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数NA个
C.7.8gNa2O2与过量水反应转移电子数为0.1NA
D.由1mol CH3COONa和 少量CH3COOH形成的中性溶液中,CH3COO﹣数目为NA个
少量CH3COOH形成的中性溶液中,CH3COO﹣数目为NA个
查看答案和解析>>
科目: 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
把200 mL NH4HCO3和Na2CO3的混合溶液分成二等份,取一 份加
份加 入含a mol氢氧化钠的溶液加热,恰好使NH4+完全转化为NH3逸出,另取一份加入含b molHCl的盐酸恰好反应完全生成CO2,则该混合溶液中c(Na+)为
入含a mol氢氧化钠的溶液加热,恰好使NH4+完全转化为NH3逸出,另取一份加入含b molHCl的盐酸恰好反应完全生成CO2,则该混合溶液中c(Na+)为
A.(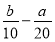 )mol/L B.(2b-a) mol/L
)mol/L B.(2b-a) mol/L
C.(5b-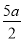 )mol/L D.(10
)mol/L D.(10 b-5a) mol/L
b-5a) mol/L
查看答案和解析>>
科目: 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是
A.在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32-
B.含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+
查看答案和解析>>
科目: 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+。下列叙述不正确的是
A.氧化产物为Cl2
B.氧化剂与还原剂的物质的量之比为1∶2
C.若有3mol H2O生成,则反应中有2mol电子转移
D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移
查看答案和解析>>
科目: 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.任何化学反应都伴随着能量变化
B.放热反应的反应速率总是大于吸热反应的反应速率
C.离子化合物中一定含有离子键,可能含有共价键
D.强 电解质与弱电解质的区别就是电解质在水溶液中是否完全电离
电解质与弱电解质的区别就是电解质在水溶液中是否完全电离
查看答案和解析>>
科目: 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
饱和氯水中存在如下平衡:①Cl2+H2O H++Cl-+HClO ;②HClO
H++Cl-+HClO ;②HClO H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是( )
H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是( )
A.加入CaCO3悬浊液,CaCO3的溶解平衡向右移动
B.加入澄清石灰水,c(H+)一定减小
C.加入一定量NaOH溶液后,溶液中离子浓度的关系可能为c(Cl-) +c(ClO-) =c(Na+)
D.通入过量Cl2,①、②均向右移动,溶液pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com