
科目: 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:选择题
反应3A(g)+B(g) 2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
A.v(A)=1.5 mol·L-1·s-1
B.v(C)=0.5 mol·L-1·s-1
C.v(D)=0.6 mol·L-1·s-1
D.v(B)=0.4 mol·L-1·s-1
查看答案和解析>>
科目: 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:选择题
NH4HS(s) NH3(g)+H2S(g)在一定温度下达到平衡,下列情况不能使平衡发生移动的是
NH3(g)+H2S(g)在一定温度下达到平衡,下列情况不能使平衡发生移动的是
A.温度、容积不变,充入NH3
B.温度、容积不变时,充入SO2气体
C.充入N2,保持压强不变
D.移走一部分NH4HS固体
查看答案和解析>>
科目: 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:选择题
298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+ 立即被还原成Fe2+。据此某学习小组设计如图所示的原电池装置。下列有关说法正确的是

A.正极反应为:Zn – 2e-→Zn2+
B.盐桥中K+向右池移动
C.Pt电极上有气泡出现
D.左烧杯中溶液的红色变浅
查看答案和解析>>
科目: 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:选择题
某学习小组为了探究 BrO3- + 5Br- + 6H+ = 3Br2 + 3H2O 反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表,下列结论不正确的是
实验编号 相关数据 | ① | ② | ③ | ④ | ⑤ |
c(H+)/ mol · L-1 | 0.008 | 0.008 | 0.004 | 0.008 | 0.004 |
c(BrO3-)/ mol· L-1 | 0.001 | 0.001 | 0.001 | 0.002 | 0.002 |
c(Br-)/ mol· L-1 | 0.10 | 0.20 | 0.20 | 0.10 | 0.40 |
v / mol· L-1· s-1 | 2.4×10-8 | 4.8×10-8 | 1.2×10-8 | 4. 8×10-8 | v1 |
A.若温度升高到40℃,则反应速率增大
B.实验②、④,探究的是c(BrO3-)对反应速率的影响
C.若该反应速率方程为v = k ca(BrO3-)cb(Br-)cc(H+)(k为常数),则c = 2
D.实验⑤中,v1 = 4.8×10-8 mol· L-1· s-1
查看答案和解析>>
科目: 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:填空题
某同学设计了一个甲醇(CH3OH)燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图1:
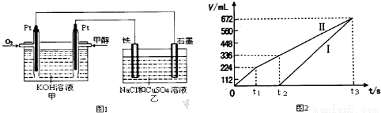
(1)25℃,1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为 。
(2)写出甲中通入甲醇这一极的电极反应式 。
(3)铁电极上反应的现象为:先有红色的物质析出,后 。
石墨电极上产生的气体是 。
(4)理论上乙中两极所得气体的体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积)原混合溶液中CuSO4的物质的量浓度 mol·L-1。(假设溶液体积不变)
查看答案和解析>>
科目: 来源:2015-2016学年安徽省宣城、郎溪、广德三校高二上期中联考化学试卷(解析版) 题型:选择题
已知:强酸强碱的稀溶液发生中和反应的中和热△H=-57.3kJ/mol,C2H6的燃烧热△H=-1559.8kJ/mol。
A.H2CO3(aq) + 2NaOH(aq) = Na2CO3(aq) + 2H2O(l) △H=-114.6kJ/mol
B.2C2H6(g) + 7O2(g) = 4CO2(g) + 6H2O(l) △H=-3119.6kJ/mol
C.NaHCO3(aq) + NaOH(aq) = Na2CO3(aq) + H2O(l) △H=-57.3kJ/mol
D.C2H6(g) + 7/2O2(g) = 2CO2(g) + 3H2O(g) △H=-1559.8kJ/mol
查看答案和解析>>
科目: 来源:2015-2016学年安徽省宣城、郎溪、广德三校高二上期中联考化学试卷(解析版) 题型:选择题
下列关于可逆反应H2(g) + I2(g)  2HI(g)在一定温度与体积条件下达到平衡的判断正确的是
2HI(g)在一定温度与体积条件下达到平衡的判断正确的是
A.每断裂1mol H-H键的同时断裂1mol I-I键
B.每断裂1mol I-I键的同时生成2mol H-I键
C.每消耗1molH2的同时消耗2molHI
D.压强不发生改变
查看答案和解析>>
科目: 来源:2015-2016学年安徽省宣城、郎溪、广德三校高二上期中联考化学试卷(解析版) 题型:选择题
可逆反应2SO2(g) + O2  2SO3(g) △H <0,达到平衡后,在其他条件不变的情况下改变下列条件,SO2转化率减小的是
2SO3(g) △H <0,达到平衡后,在其他条件不变的情况下改变下列条件,SO2转化率减小的是
A.降低温度
B.保持压强充入N2
C.保持体积不变,增加O2
D.增大压强
查看答案和解析>>
科目: 来源:2015-2016学年安徽省宣城、郎溪、广德三校高二上期中联考化学试卷(解析版) 题型:填空题
在一定体积的密闭容器中,进行如下化学反应:
CO2(g) + H2(g)  CO(g) + H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g) + H2O(g),其化学平衡常数K和温度T的关系如下表:
T/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为 反应(填“吸热”、“放热”)。
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离出CO气体
b.适当升高温度
c.增大CO2的浓度
d.选择高效催化剂
(3)能判断该反应是否达到化学平衡状态的依据是 (多选不得分)。
A.容器中压强不变
B.混合气体中 c(CO)不变
C.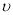 正(H2)=
正(H2)= 逆(H2O)
逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
(5)若在(4)所处的温度下,在1L的密闭容器中,加入2molCO2和3molH2充分反应达平衡时,H2的物质的量为 ,CO2的物质的量为 。
A.等于1.0mol
B.大于1.0mol
C.大于0.5mol,小于1.0mol
D.无法确定
查看答案和解析>>
科目: 来源:2016届山东省高三上学期期中阶段测试化学试卷(解析版) 题型:选择题
下列金属冶炼的反应原理正确的是
A.2Al2O3 +3C  4Al+3CO2↑
4Al+3CO2↑
B.MgO + H2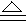 Mg+H2O
Mg+H2O
C.Fe3O4+4CO 3Fe+4CO2
3Fe+4CO2
D.2HgO 2Hg + O2↑
2Hg + O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com