
科目: 来源:同步题 题型:填空题
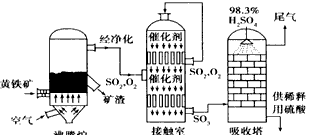
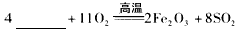
查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
科目: 来源:浙江省期中题 题型:单选题
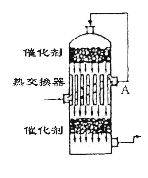
查看答案和解析>>
科目: 来源:浙江省期中题 题型:单选题
查看答案和解析>>
科目: 来源:山东省模拟题 题型:填空题
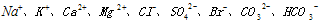 等离子。
等离子。 查看答案和解析>>
科目: 来源:河南省模拟题 题型:填空题
 SO3(g) △H=-98.3kJ/mol放出的热量能在生产过程中得到充分利用,则每生产1t98%的硫酸只需外界提供(或可向外界输出)____kJ能量。
SO3(g) △H=-98.3kJ/mol放出的热量能在生产过程中得到充分利用,则每生产1t98%的硫酸只需外界提供(或可向外界输出)____kJ能量。 
查看答案和解析>>
科目: 来源:模拟题 题型:填空题

查看答案和解析>>
科目: 来源:模拟题 题型:填空题

查看答案和解析>>
科目: 来源:陕西省模拟题 题型:填空题
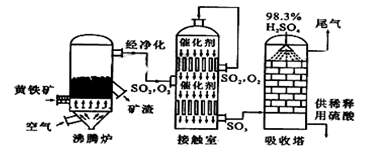
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.用浓硫酸吸收不形成酸雾,吸收速率快 |
| B.用水吸收生成的酸雾多,影响吸收 |
| C.用水不能吸收SO3 |
| D.用浓硫酸吸收可以得到更浓的硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com