
科目: 来源:2016届西藏拉萨中学高三上学期第二次月考化学试卷(解析版) 题型:填空题
(14分)甲醇是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
① CO(g) + 2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
② CO2(g) + 3H2(g) CH3OH(g)+ H2O(g) △H2
CH3OH(g)+ H2O(g) △H2
③ CO2(g) + H2(g) CO(g) + H2O(g) △H3
CO(g) + H2O(g) △H3
回答下列问题:
(1)已知
化学键 | H-H | C-O | C=O | H-O | C-H |
E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
则△H1= kJ.mol-1
(2)图1中能正确表现反应①的平衡常数K随温度变化关系的曲线为 (填曲线标记字母),判断理由是 。

(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而 (填“增大”或“减小”)原因是 。
图2中的压强由大到小为 ,判断理由是 。
查看答案和解析>>
科目: 来源:2016届西藏拉萨中学高三上学期第二次月考化学试卷(解析版) 题型:填空题
(15 分)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,根据要求解决下列问題:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为 (3分)。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为 (3分)。
②溶液X中大量存在的阴离子有__________________。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
a.水 b.碱石灰 c.浓硫酸 d.饱和食盐水
(3)为了测定混合气体中ClO2的含量,我们通常用酸化的KI溶液与之反应。
①请写出ClO2与碘化钾反应的离子方程式为 (3分)。
②如果反应过程中共消耗了 0.04 mol的KI,则此混合气体中ClO2的质量为________克。
查看答案和解析>>
科目: 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA
B.电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数为0.2NA
C.常温下,1.0L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
D.将100mL0.1mol·L -1 的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
查看答案和解析>>
科目: 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
常温下,在下列指定条件的各溶液中,一定能大量共存的离子组是
A.中性溶液中: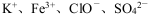
B.pH<7的溶液中:
C.加入金属镁能产生H2的溶液中:
D.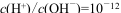 的溶液中:
的溶液中: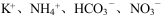
查看答案和解析>>
科目: 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g) +Y(g)  3Z(g),反应过程持续升高温度,测得X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g),反应过程持续升高温度,测得X的体积分数与温度的关系如图所示。下列推断正确的是
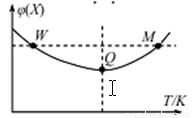
A.Q点时,Y的转化率最大
B.升高温度,平衡常数增大
C.W点X的正反应速率等于M点X的正反应速率
D.平衡时充入Z,达到新平衡时Z的体积分数增大
查看答案和解析>>
科目: 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
下列关系式中,正确的是
A.等浓度等体积的CH3COOH和CH3COONa溶液混合:c(CH3COO- )+c(OH -)=c(H+)+c(CH3COOH)
B.常温下,0.1 mol·L-1 HA溶液与0.1 mol·L NaOH溶液等体积完全反应时,溶液中一定存在:c(Na+)=c(A- )>c(OH )=c(H+)
C.常温下,0.1 mol·L-1 Na2S溶液中存在:c(OH- )=c(H+)+c(HS- )+c(H2S)
D.常温下,将0.1 mol·L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到5.0时,溶液中c(CHCOO-)/c(CHCOOH)的值增大到原来的100倍
查看答案和解析>>
科目: 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:填空题
(本小题满分14分)
T1温度下,体积为 2L的恒容密闭容器,加入4.00mol X,2.00mol Y,发生化学反应 2X(g)+Y(g)
 3M(g)+N(s) △H<0。部分实验数据如表格所示。
3M(g)+N(s) △H<0。部分实验数据如表格所示。

(1)前500s反应速率v(M)= _____________,该反应的平衡常数K=_____________。
(2)若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是____________(填序号)
A.X的消耗速率与M的消耗速率相等
B.混合气体的平均相对分子质量不变
C.v(Y)与v(M)的比值不变
D.固体的总质量不变
(3)该反应达到平衡时某物理量随温度变化如下图所示。纵坐标可以表示的物理量有哪些_____________。
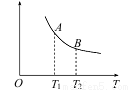
A.Y的逆反应速率
B.M的体积分数
C.混合气体的平均相对分子质量
D.X的质量分数
(4)反应达到平衡后,若再加入3.00molM,3.00molN,下列说法正确的是_____________。
A.平衡不移动
B.重新达平衡后,M的体积分数小于50%
C.重新达平衡后,M的物质的量浓度是原平衡的1.5倍
D.重新达平衡后,Y的平均反应速率与原平衡相等
E.重新达平衡后,用X表示的v(正)比原平衡大
(5)若容器为绝热恒容容器,起始时加入4.00molX,2.00molY,则达平衡后M的物质的量浓度_____________1.5mol/L(填“>”、“=”或“<”),理由是__________________。
查看答案和解析>>
科目: 来源:2016届四川省成都市高三上学期期中考试理综化学试卷(解析版) 题型:填空题
(本小题满分15分)
参考下列图表和有关要求回答问题:
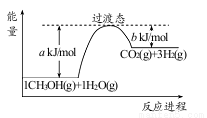
(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2。右图是该过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是_____________(填“增大”、“减小”、“不变”),反应热△H的变化是_____________(填“增大”、“减小”、“不变”)。请写反应进程出CH3OH(g)和H2O(g)反应的热化学方程式_____________。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:CH3OH(g)+1/2O2(g) 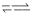 CO2(g)+2H2(g) △H=c kJ/mol又知H2O(g)
CO2(g)+2H2(g) △H=c kJ/mol又知H2O(g) 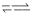 H2O(l) △H=d kJ/mol。则甲醇燃烧生成液态水的热化学方程式为_____________。
H2O(l) △H=d kJ/mol。则甲醇燃烧生成液态水的热化学方程式为_____________。
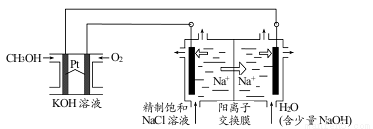
(3)以CH3OH燃料电池为电源电解法制取ClO2。二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①CH3OH燃料电池放电过程中,通入 O2的电极附近溶液的pH_____________,负极反应式为_____________。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ClO2。阳极产生 ClO2的反应式为_____________。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_____________mol。
查看答案和解析>>
科目: 来源:2016届河南省林州市高三上学期9月质检化学试卷(解析版) 题型:选择题
向含有c(FeCl3)=0.2 mol·L-l、c(FeCl2)=0.1 mol·L-l的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3 nm的金属氧化物,下列有关说法中正确的是
A.该分散系的分散质为Fe2O3
B.加入NaOH时发生的反应可能为:Fe2+ + 2Fe3+ + 8OH- = Fe3O4 + 4H2O
C.在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷
D.可用过滤的方法将黑色金属氧化物与Na+分离开
查看答案和解析>>
科目: 来源:2016届河南省林州市高三上学期9月质检化学试卷(解析版) 题型:选择题
下列操作中,后者最终能被漂白的是
A.将干燥的氯气与红色鲜花充分接触 B.将H2O2加入到KMnO4溶液中
C.将足量SO2通入紫色石蕊试液中 D.将漂白液加入到Fe2 (SO4)3溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com