
科目: 来源:2016届安徽省皖南八校高三上学期第一次联考化学试卷(解析版) 题型:实验题
冰晶石(Na3 AlF6)难溶于水,广泛应用于铝的冶炼。工业上用萤石(CaF2)为原料生产Na3 AlF6:
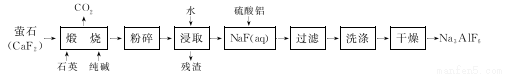
回答下列问题:
(1)在铝的冶炼中,Na3AlF6的作用是 。
(2)煅烧时总反应的化学方程式为 ,用水浸取后残渣的主要成分是
,用水浸取后残渣的主要成分是
(3)煅烧后的固体在浸取前进行粉碎的目的是 ,为达到相同目的,常温浸取时还可采取的措施是 。
(4)写出向NaF溶液中加入硫酸铝溶液发生反应的离子方程式:__ __。NaF溶液呈碱性,用离子方程式表示其原因: ,因此在按化学计量加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,否则可能产生副产物
(5)97.5 kg含CaF2 80%萤石(杂质不含氟元素)理论上可生产Na3 AlF6 kg(设生产过程中的每一步含氟物质均完全转化)。
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列实验操作或记录正确的是
A.常温常压下测得1 mol N2的质量为28 g
B.用量筒测得排水法收集制得的氢气体积为50.28 mL
C.用两只250 mL的容量瓶配制0.1 mol·L-1500 mL的NaOH溶液
D.用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期10月月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y 的次外层电子数是最外层的1/3,ZX2是一种储氢材料,W与Y属于同一主族。下列叙述正确的是
A.原子半径:rW>rZ>rY
B.Y形成的离子与W形成的离子的电子数不可能相同
C.化合物X2Y、ZY、WY3 中化学键的类型相同
D.由X、Y、Z、W组成的化合物的水溶液可能显酸性
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期10月月考化学试卷(解析版) 题型:填空题
(15分)发生在天津港“8·12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注。
(1)为了减少空气中SO2的排放,常采取的措施是将煤转化为清洁气体燃料。
已知:①H2(g)+1/2O2(g)==H2O(g) ΔH1=-241.8 kJ·mol-1
②C(s)+1/2O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1
则焦炭与水蒸气反应生成CO的热化学方程式为: 。
(2)由于CaC2、金属钠、金属钾等物质能够跟水反应给灾后救援工作带来了很多困难。如果在实验室,你处理金属钠着火的方法是 。
(3)事故发生后,爆炸中心区、爆炸区居民楼周边以及海河等处都受 到了严重的氰化物污染。处理NaCN的方法是:用NaClO在碱性条件下跟NaCN反应生成无毒害的物质,试写出该反应的离子反应方程式 。
(4)电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO的原理如图所示,电源正极为 (填“a”或“b”);若总反应为4NO3-+4H+====5O2↑+2N2↑+2H2O,则阴极反应式为 。

(5)欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去。
已知在常温下:Ksp[Fe(OH)2]= 1×10-15、Ksp[Fe(OH)3]= 1×10-38 、
Ksp[Cr(OH)3]= 1×10-23 ,当离子浓度在1×10-5mol/L以下时认为该离子已经完全沉淀,请回答:
① 相同温度下Fe(OH)3的溶解度 Cr(OH)3的溶解度(填“>”、“<”或“=”)
② 浓度为0.1mol/L的Fe2+与10. 0mol/L Cr3+同时生成沉淀的pH范围是 。
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期10月月考化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
A、B、C、D、E为原子序数依次增大的四种元素,A的价电子层中的未成对电子有3个,B的最外层电子数为其内层电子数的3倍,C、D为同周期元素,C元素基态原子的3p轨道上有4个电子,D元素最外层有一个未成对电子,E位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。回答下列问题:
(1)D原子的核外电子排布式为 ,E的价层电子轨道示图为_________________。
(2)单质B有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;
(3)A、B、C中第一电离能最大的是________(填元素符号),其中A的氢化物(AH3)分子中,A原子轨道的杂化类型是 。
(4)化合物D2B的立体构型为 ,单质D与湿润的Na2CO3反应可制备D2B,其化学方程式为 .
(5)E与C所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,E离子的数目为 。
②该化合物的化学式为 。
查看答案和解析>>
科目: 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
可能存在的第119号未知元素,有人称为“类钫”,它位于碱金属族,根据周期表结构及元素性质变化趋势,下列关于碱金属某些元素原子的结构和性质的判断,错误的是
①锂与水反应比钠剧烈
②碱金属单质都需要密封保存在煤油中
③锂的氧化物暴露在空气中易吸收二氧化碳
④锂的阳离子的最外层电子数和钠的相同
⑤“类钫”单质是强还原剂
⑥“类钫”在化合物中是+1价
⑦“类钫”单质的密度大于l g·cm-3⑧“类钫”单质有较高的熔点
A.①②④⑧ B.①②③⑦ C.③④⑤⑧ D.①③④⑦
查看答案和解析>>
科目: 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
固体NH5属离子化合物。它与水反应的方程式为:NH5+H2O=NH3 ? H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气。下列有关NH5叙述正确的是
A.1 mol NH5中含有5NA个N—H键
B.NH5中N元素的化合价为-5价
C.与水反应时,原理和NaH与水反应相同
D.与乙醇反应时,NH5被还原
查看答案和解析>>
科目: 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
实验是解决化学问题的基本途径,下列有关实验的叙述不正确的是
A.240 mL 0.2 mol·L-1的NaOH溶液配制:需要使用天平、烧杯、250 mL容量瓶等仪器
B.除去Cu粉中的CuO,可向混合物中滴加适量稀硫酸再过滤
C.为增强氯水的漂白性,向其中加入碳酸钙
D.为使0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50克水
查看答案和解析>>
科目: 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
下列热化学方程式书写正确的是
A、C(s)+O2(g)==CO2(g);△H=+393.5kJ/mol
B、2SO2+O2==2SO3;△H= —196.6kJ/mol
C、H2(g)+1/2O2(g)==H2O(l);△H= —285.8kJ/mol
D、2H2(g)+O2(g)==2H2O(l);△H= —571.6KJ
查看答案和解析>>
科目: 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:填空题
(10分)化学在能源开发与利用中起着十分关键的作用。氢气是一种新型的绿色能源,又是一种重要的化工原料。
氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行如图所示的实验(图中所用电极均为惰性电极):

(1)对于氢氧燃料电池,下列叙述不正确的是________。
A.a电极是负极,OH-移向负极
B.b电极的电极反应为:O2+2H2O+4e-===4OH-
C.电池总反应式为:2H2+O2 2H2O
2H2O
D.电解质溶液的pH保持不变
E.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(2)上图右边装置中盛有AgNO3溶液,当氢氧燃料电池工作一段时间后,AgNO3溶液的pH_____________(填“增大”、“减小”或“不变”)。
(3)已知甲醇的燃烧热ΔH=-726.5 kJ/mol,在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为_______________,正极的反应式为______________。
理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为__________(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com