
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
根据原子结构及元素周期律的知识,下列推断正确的是
A、同主族元素含氧酸的酸性随核电荷数的增加而减弱
B、核外电子排布相同的微粒化学性质也相同
C、 得电子能力相同
得电子能力相同
D、 半径逐渐减小
半径逐渐减小
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A. Z为0.3mol/L B. Y2为0.4mol/L
C. X2为0.2mol/L D. Z为0.4mol/L
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
三种气体X、Y、Z的相对分子质量关系为Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
A.三种气体密度最小的是X
B.分子数目相等的三种气体,质量最大的是Y
C.若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1 mol
D.20 ℃时,若2 mol Y与1 mol Z体积相等,则Y、Z气体所承受的压强比为2∶1
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
向恒温、恒容(2L)的密闭容器中充入2mol X和一定量的Y,发生反应:2X(g) +Y(g)  2Z(g) ΔH = - Q(Q =197.74kJ/mol),4min后达到平衡,这时c(X) =0.2 mol·L-1,且X与Y的转化率相等。下列说法中不正确的是
2Z(g) ΔH = - Q(Q =197.74kJ/mol),4min后达到平衡,这时c(X) =0.2 mol·L-1,且X与Y的转化率相等。下列说法中不正确的是
A.达到平衡时,再充入1molX,该反应的Q变大
B.用Z表示4min内的反应速率为0.2mol/(L·min)
C.再向容器中充入1molZ,达到新平衡,v(X) ∶v(Y) =2∶1
D.该反应在高温下不一定能自发进行
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
可逆反应① 、②
、② 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:

下列判断正确的是:
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时X的转化率为5/11
D.在平衡(I)和平衡(II)中的M的体积分数相同
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解)。则电解过程中转移电子的物质的量为
A.0.4 mol B.0.5 mol C.0.6 mol D.0.8 mol
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
已知:2SO2(g) +O2(g)  2SO3(g) △H=—196.6kJ·mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是
2SO3(g) △H=—196.6kJ·mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是
注:t1~t2、t3~t4、t5之后各时间段表示达到平衡状态①、②、③。
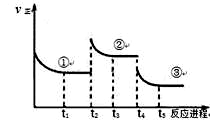
A.t2~t3时间段,平衡向逆反应方向移动
B.平衡状态①和②,平衡常数K值相同
C.平衡状态①和②,SO2转化率相同
D.t4时刻改变的条件是减小压强
查看答案和解析>>
科目: 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:填空题
(14分)铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述________________(填装置序号)装置原理进行防护;装置③中总反应的离子方程式为______________________。
(2)用CH4或其他有机物、O2为原料可设计成原电池,以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为___________________________。
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。

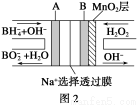
图2电池负极区的电极反应为_________________________;若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现_____________色,C位置的电极反应式为___________________若用KI?淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是__________(填A或B)电极。
(4)广西治理龙江河镉(Cd2+)污染时,先向河中投入沉淀剂将Cd2+转化为难溶物,再投入氯化铝,试说明氯化铝的作用_______________________________(用必要的离子方程式和文字进行解释)。
查看答案和解析>>
科目: 来源:2016届甘肃省高三上学期第二次月考理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列应用中利用了物质氧化性的是
A.明矾净化水 B.纯碱去油污 C.食醋除水垢 D.漂白粉漂白织物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com