
科目: 来源:江苏高考真题 题型:填空题
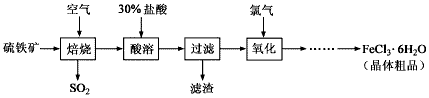
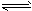 2SO3(g),该反应的平衡常数表达式为
2SO3(g),该反应的平衡常数表达式为查看答案和解析>>
科目: 来源:福建省高考真题 题型:填空题
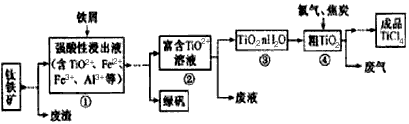
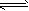 Fe3++H2O的平衡常数K=___________。
Fe3++H2O的平衡常数K=___________。
查看答案和解析>>
科目: 来源:上海高考真题 题型:填空题
查看答案和解析>>
科目: 来源:陕西省模拟题 题型:填空题
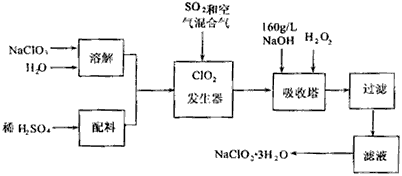
查看答案和解析>>
科目: 来源:同步题 题型:填空题
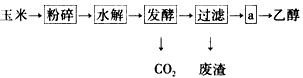
查看答案和解析>>
科目: 来源:同步题 题型:填空题
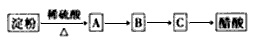
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
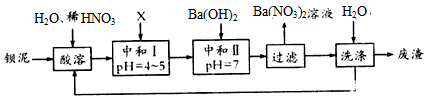
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
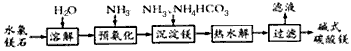
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
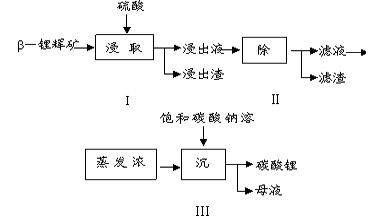
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
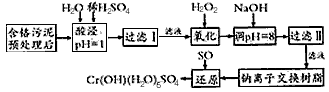

 Na2Cr2O7+
Na2Cr2O7+ SO2+
SO2+  H2O=
H2O= Cr(OH)(H2O)5SO4+
Cr(OH)(H2O)5SO4+ Na2SO4;
Na2SO4;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com