
科目: 来源:2015-2016学年河南省高二上学期第一次月考化学试卷(解析版) 题型:选择题
在密闭容器中进行反应:X2(g)+Y2(g) 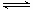 2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A.Y2为0.15mol/L B.Z为0.2mol/L
C.X2为0.3mol/L D.Z为0.4mol/L
查看答案和解析>>
科目: 来源:2015-2016学年河南省高二上学期第一次月考化学试卷(解析版) 题型:填空题
反应mA+nB pC在某温度下达到平衡。
pC在某温度下达到平衡。
(1)若A、B、C都是气体,减压后v正小于v逆,则m、n、p的关系是______ 。
(2)若在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为___________态。
(3)若A为液体,C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向________(填“正反应”或“逆反应”)方向移动。
(4)若升高温度,A物质的转化率增大,则该反应为________(“吸热”或“放热”)反应。
查看答案和解析>>
科目: 来源:2015-2016学年福建省福安市高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.原电池是把电能转化为化学能的装置
B.原电池中电子流入的一极是正极,发生还原反应
C.铜锌原电池中电子由锌电极经过溶液到铜电极
D.原电池中的阳离子向负极移动
查看答案和解析>>
科目: 来源:2015-2016学年福建省福安市高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是
A.石油、沼气、天然气、植物油都属于可再生能源
B.水蒸气变为液态水时放出的能量就是该变化的反应热
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
科目: 来源:2015-2016学年福建省福安市高二上学期第一次月考化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是
A.X、Y元素的金属性 X<Y
B.一定条件下,W单质可以将Z单质从其氢化物中置换出来
C.一定条件下,Z单质与W的常见单质直接生成ZW2
D.Y的最高价氧化物对应的水化物能溶于稀氨水
查看答案和解析>>
科目: 来源:2015-2016学年福建省福安市高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列有关试剂的保存方法正确的是
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④锂保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中
A.①③⑤ B.②③⑤ C.②④⑤ D.①③④
查看答案和解析>>
科目: 来源:2015-2016学年福建省福安市高二上学期第一次月考化学试卷(解析版) 题型:填空题
(12分)硫及其化合物在工业生产中有重要的应用,它们性质的研究对工业生产有重要的指导意义。
(1)2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示。
2SO3(g),反应过程的能量变化如图所示。

已知1 mol SO2(g)氧化为1 mol SO3(g)放出的热量为99 kJ。请回答下列问题:
①图中E表示_____________,E的大小对该反应的反应热有无影响?_______________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____________,理由是_____________;
②图中ΔH=____________kJ·mol-1;
(2)下图表示在密闭容器中反应2SO2+O2 2SO3 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。
2SO3 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。

①a b过程中改变的条件可能是 ;
②b c过程中改变的条件可能是 ;
③若增大压强时,反应速率变化情况画在c~d处。
查看答案和解析>>
科目: 来源:2015-2016学年福建省福安市高二上学期第一次月考化学试卷(解析版) 题型:填空题
(17分)甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料。甲醇在各个领域有着广泛的应用。
(1)实验测得:32 g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出726.4 kJ的热量,试写出甲醇燃烧的热化学方程式:_________________________。
(2)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池。下图是一个化学过程的示意图。2CH3OH+3O2+4KOH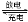 K2CO3+6H2O
K2CO3+6H2O
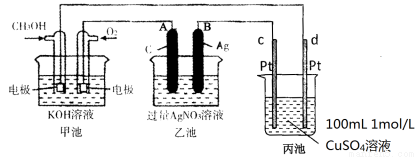
①A(石墨)电极的名称是 。
②通入O2的电极的电极反应式是________________
③写出通入CH3OH的电极的电极反应式是 。
④乙池中反应的化学方程式为 。
⑤当电路中通过0.01mol电子时,丙池溶液的C(H+) = mol/L(忽略电解过程中溶液体积的变化)。
(3)合成甲醇的主要反应是:2H2(g)+ CO(g) CH3OH(g) △H=—90.8 kJ·mol—1。
CH3OH(g) △H=—90.8 kJ·mol—1。
①在恒温恒容条件下,充入一定量的H2和CO,发生反应2H2(g)+ CO(g) CH3OH(g)。则该反应达到平衡状态的标志有
CH3OH(g)。则该反应达到平衡状态的标志有
a.混合气体的密度保持不变 b.混合气体的总压强保持不变
c.CO的质量分数保持不变 d.甲醇的浓度保持不变
e.v正(H2)= v逆(CH3OH) f.v(CO)= v(CH3OH)
②要提高反应2H2(g)+ CO(g) CH3OH(g)中CO的转化率,可以采取的措施是:
CH3OH(g)中CO的转化率,可以采取的措施是:
a.升温 b.加入催化剂
c.增加CO的浓度 d.加入H2
e.加入惰性气体 f.分离出甲醇
查看答案和解析>>
科目: 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:选择题
用14C标记的一种C60羧酸衍生物,在特定条件下会断裂DNA抑制艾滋病毒的繁殖。以下有关14C的叙述正确的是
A.与12C60的碳原子化学性质不同 B.与15N含的中子数相同
C.与12C60互为同素异形体 D.与12C、13C互为同系物
查看答案和解析>>
科目: 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:选择题
下列用水能鉴别的一组物质是
A.乙酸乙酯、甘油、硝基苯 B.乙醇、甘油、四氯化碳
C.乙酸乙酯、苯、乙醇 D.苯、四氯化碳、硝基苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com